浏览量 2227


文章作者:
Parexel精鼎医药执行副总裁、首席商务官兼首席战略官Peyton Howell
全球的监管机构、政策制定者和临床研究人员都知道真实世界研究能协助做出明智的监管和市场准入决策。尽管如此,对于许多市场而言,管理真实世界数据(RWD)和真实世界证据(RWE)的法规仍在起步阶段。真实世界证据是指,对从真实世界环境(即正常临床实践而非对照试验)中获取的数据进行优化分析而获得的证据(在本文中,我们主要使用术语RWE,除非需要使用RWD阐明内容及介绍背景)。
RWE应用比较缓慢的主要原因是它与完善的临床试验过程存在固有差异及其相对新颖性。它需要通过专门的运作模式,以克服在常规真实世界环境中收集数据时或为新用途访问现有数据时所面临的困难。但是,RWE的应用速度正在加快。数据科学家正在优化诸如人工智能(AI)、机器学习(ML)和自然语言处理(NLP)这样的技术,以更好地提取和挖掘RWD,同时监管机构正在制定关于RWD访问、使用、存储和隐私的政策。
本文将介绍中日两国如何使用RWD/RWE;为更好地利用强大的RWD/RWE做出更明智的决策,两国正在开展的重大项目;以及生物制药公司需要考虑的重要因素。
那些希望在医疗保健系统中使用RWE的国家/地区面临着诸多巨大障碍。首先是数据本身,与临床试验数据不同,RWE相关数据有着各种来源,这些来源的数据可能不完整、不一致、难以获取,例如,电子病历(EMR)、保险理赔数据库、实验室数据、全国民调、药品和疾病登记,以及移动设备生成的数据。
更复杂的是,患者数据的采集格式不规范。来自医院和其他护理机构、EMR系统、保险理赔系统和登记系统的数据集在输入方案、术语或详细程度方面并不统一。为汇总数据以进行有意义的分析,研究人员必须使用专门的方法来映射和组织数据,对数据编码并建立关联。
RWE源自对原始和/或二手RWD的分析、解读和转换。原始RWD是指出于特定目的(如前瞻性观察研究),需要从医生或患者处实时采集的数据。二手RWD是指因其他目的而收集且可“再用于”后续分析的数据。大多数分析需要利用多个数据源(例如,多个辅助数据集或主要和辅助数据的组合),以充分解决当前的研究问题。
要获得强大的RWE,需要访问各种数据类型,了解有意义的指标,以及识别最佳数据和将不同来源数据相关联的能力。医学信息学、数据科学、临床研究、流行病学、生物统计学、AL/ML、NLP、编程及合作研究方面的专业知识都是必不可少的,这是成功管理这些项目所必需的运营专业知识。大多数国家/地区在这些领域都缺乏训练有素的专业研究人员。
正确解读和分析准确的RWD能够提供有价值的RWE;若数据质量较低且分析方法存在缺陷,则提供的证据难以解读,无法解决关键的研究问题。
RWE有潜力填补随机临床试验(RCT)结果与现实生活环境中所见结果之间的差距,在现实生活环境中,依从性、合并症和其他混杂因素可能且通常不同。RWE在以下领域非常有用:
-
向监管人员和支付方提供令人信服的证据,就处方定位和定价提供支持,完成上市后承诺,提供新疗法报销依据并加快药物审批。
-
帮助开发人员做出明智的决策,它可以让他们更好地了解产品用途、实践模式以及对于提供最佳产品开发和商业化支持至关重要的其他因素。RWE可以在患者选择标准方面提供见解,确定未得到满足的医疗需求并优化生命周期管理策略。RWE还可以帮助识别并描述参与治疗的医师和患者,并阐明疾病的自然病史和治疗护理实践标准,为临床试验设计提供信息。
-
提供市场竞争优势,它能协助实现产品差异化,与该领域的专家建立密切联系,让患者了解更多信息,提高患者的意识,并帮助临床医生制定治疗决策。
在努力应对提供有价值(即具有有用信息且切实可行)RWE方面的挑战过程中,临床研究人员已开始设计压力测试技术解决及研究方案。
比如,利用“数据湖”执行的新型混合研究可以帮助调整各个地区的商业策略。最近,Parexel与客户合作,共同构建了一个关于复发缓解型多发性硬化症(MS)患者持久性应答的可扩展纵向数据集。该客户设计了一种强大的算法来识别MS子类型,但他们需要多个地区的应答证据来帮助他们将产品推向市场。
Parexel在五个国家/地区开展了适当RWD来源的可行性研究,并专门构建了一个数据湖,为深度分析提供技术基础架构。该解决方案将不同的数据源(每个数据源的数据管理策略有所相同)与定制方法进行了结合,能够将来自各个数据源的数据加载并转换到数据湖中。
除了创新型混合研究外,申办方和监管机构正尝试在正式临床试验中采用基于 RWE的合成/外部对照组。Parexel目前正在与一个客户合作,计划通过在II期单臂研究中将RWE合成对照组用作对照组,帮助客户向监管部门递交肿瘤疗法上市申请。
Parexel和产品开发人员与美国FDA合作开发了研究设计并审查研究进展情况。在美国,结合使用了辅助数据源和图表审查,在欧洲则只使用了图表审查。技术合作伙伴还提供了创新平台,用以汇总美国患者数据。
了解如何从高质量RWE中获取最大价值是一个持续的过程,需要采用先进的技术和前沿的研究方法。
中国和日本分别是世界第二大和第三大生物制药市场,在这两个国家,RWE是重中之重。各个国家/地区要想制定并完善这方面的指导原则,使其适用于监管体系、生物制药行业和医疗基础设施,需要与这三方保持联系并不断创新。这样,可以获得巨大回报,因为RWE能够比传统临床研究更准确地表征疾病负担(包括未满足的需求)以及治疗的临床效益和经济影响。
这两个市场的监管环境有所不同:经过了长时间的审评,中国最近发布了试行版 RWE指导原则,而日本尚未发布官方指导原则。下面,我们来了解一下每个市场的最新构想。
全球范围内,美国FDA率先面向监管机构和申办方实施了RWE审议程序(2016年《21世纪治愈法案》有相关规定),中国紧随其后。
2018年12月,FDA发布了框架草案,其中定义了RWE审议方法并确定了关于制定指导原则草案(预计将于2021年发布)的关键因素。该框架包括关于向监管部门申报的标准,但没有临床操作标准。
在收到来自美国、加拿大、欧盟和日本制药协会等各种组织和个人对该草案的一千多条意见后,CDE于2020年1月7日发布了该文件的试行版本《真实世界证据支持药物研发与审评的指导原则(试行)》。
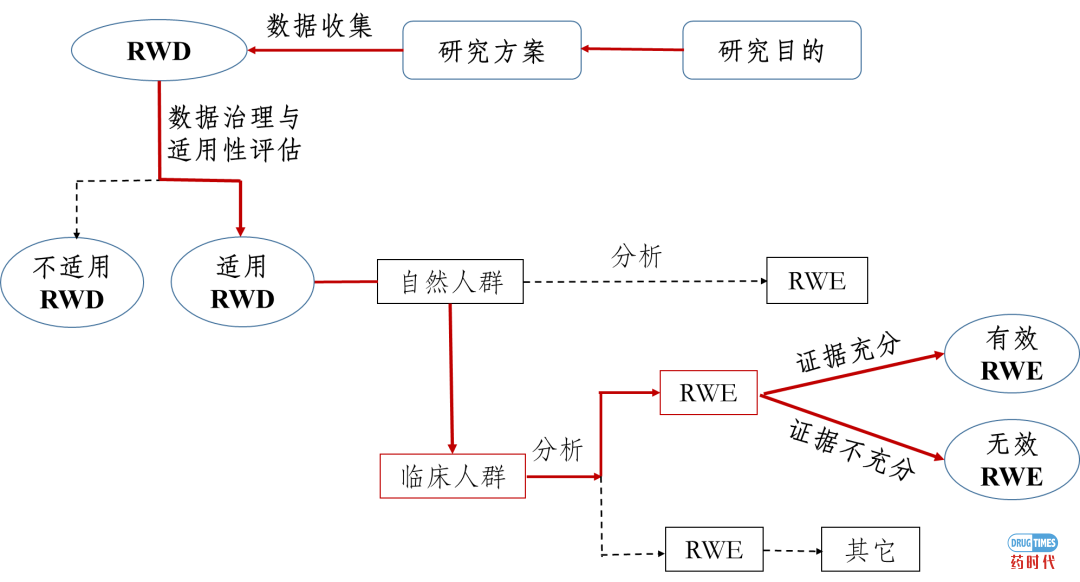
中国的试行版指导原则与FDA的相似。与FDA一样,它强调必须保证生成RWE所用数据的质量、相关性和可靠性。指导原则文件包括关于将RWD用于RWE的流程及适用情况图表(见图1)。
资料来源:《真实世界证据支持药物研发与审评的指导原则(试行)》,NMPA药品审评中心(2020年1月),第4页。
1、就新药注册提供安全性和有效性证据(包括在罕见和致命性疾病研究中采用合成对照组);
2、提供现有药品标签变更证据(例如,适应症扩展、新适应症和剂量变更);
4、用于研发传统中药(TCM)制剂;TCM在中国市场广阔,市场占比大于西药。中医会在处方中开出多种药材(通常是草药),专门为患者制定治疗方案。因此,很难通过传统的RCT方法证明安全性和有效性。
5、用于支持监管决策的其他用途,例如,就精准医学试验的设计和目标患者群体的确定提供指导。
根据试行版指导原则,使用RWE的最终目标是“精准用药”。但该文件明确指出,若根据RWE批准产品,需要就研究目标和方法“事先与监管机构进行充分沟通”。
为何中国如此关注RWE?首先,中国国内新药需求促使监管机构需要缩短境外药品评审时间,而RWE可以支持循证加速审查。其次,缺乏科学证据支持TCM的有效性,而这一紧迫问题或许可以通过RWE解决。最后,RWE与中国宣称的致力于发展“医疗大数据”的目标相辅相成。它可以在决策、合理用药以及以具有成本效益的方式应用医疗技术方面起到很好的辅助作用。
中国已开始在监管决策中采用RWE。2019年5月发布的指导原则草案指出,2018年,根据来自三项回顾性研究的有力真实世界证据,NMPA批准了安维汀(贝伐珠单抗)联合铂类药物化疗这一疗法。
尽管Parexel的全球生物制药客户对新试行版RWE指导原则的反应不一,但他们普遍对CDE修订版文件的出台表示欢迎。该文件明确说明了哪些活动在中国是具有风险的。试行版指导原则提高了监管可预测性,并确定了优先使用情况。
对于中国广大的生物技术和传统中药企业,该指导原则让他们看到了RWE可以提高药物开发效率的希望。对于以前未投资RWE的传统生物制药公司来说,CDE的认同会促使他们重新审视中国的这一领域。对于领先的RWE公司而言,可能需要根据试行版指导原则(以及详细说明实施标准的未来“行动指导原则”)更改数据收集、管理和使用的一般做法。CDE试行版文件的发布迈出了大胆的一步;需要后续的指导来有效地监管这一广大的市场。
日本在RWE方面的进展与世界许多其他地区的监管机构大体保持一致:他们尚未就细节进行全面研究。美国《二十一世纪治愈法案》中的强制性规定不存在于其他任何地区,大多数国家/地区在这一方面都非常谨慎。日本最大的顾虑之一是如何保护患者数据。
日本已经构建了强大的数据集和登记库。但是,与中国相比,日本在隐私、患者数据访问和数据商品化方面的政策(即使数据已去识别化)更加严格。
真实世界研究是一种较新的方法,因此在设计和分析方面都比随机对照试验更具挑战性。与其他国家/地区一样,日本生物制药行业和临床研究机构正在设法培养具备必要技能且训练有素的人才。
最近,Parexel已开始使用医疗信息数据库网络(MID-NET;一种由日本药品与医疗器械管理局(PMDA)管理的实时EMR数据库)和商业理赔数据库MDV。例如,Parexel已使用这两个数据库了解了日本市场上两种治疗骨质疏松的竞争药物的处方模式和应答率,并定位了拥有大量血友病A患者库、适合参与III期试验的研究中心。
RWE的未来:协助做出更明智的监管和市场准入决策,改善医疗结果
中国、日本和其他国家/地区的立法者和政策制定者均密切关注RWE,这是因为RWE能够明显改善药物开发过程,改善医疗结果并实现增值。如今,在十年前根本不存在的庞大数据集和技术将会开创一个充满希望的新时代,将关于疗法有效性和疗法使用的循证见解成为可能。
现在最需要解决的问题是,制定明确的RWE指导原则,供组织遵循。否则,生物制药公司不愿意对RWE进行投资。如上所述,这类指导原则正在制定中,但速度和方式有所不同。虽然该监管框架是拼凑而成的,但还在不断发展,它对于最终为RWE创建一种和传统临床试验一样容易理解的运作模式至关重要。
在中国、日本和其他国家/地区制定该框架的同时,生物制药公司应该提升自己的内部RWE能力,与在全球和地方层面理解RWE的组织合作,执行各公司的RWE策略。在当今商业环境中,合作非常重要,尤其是在RWE方面。必须开展广泛合作,才能访问所需的数据集,并在使用大数据方面与这些合作伙伴和思想领袖建立信任。
与监管机构和政策制定者保持联系也很重要。目前正在制定的指导原则不断变化且速度很快。了解国家层面的进展情况并积极参与其中,能够帮助监管机构和政策制定者制定切实可行的路线图。
最后,需要证明RWE能给整个医疗生态系统带来的效益。清楚说明效益并列举真实世界示例后,就能极大地促进创新。要收集RWE所需的庞大医疗数据集,需要有良好的信誉并保证将出于患者、付款人和提供者的利益妥善使用这些数据。
特别鸣谢:Parexel精鼎医药数据科学高级总监Sheng Feng对中国一节的显著贡献。
参考文献:
1、Parexel 中日两国真实世界证据圆桌会议,2019 年 9 月,与会代表包括 Parexel、各制药和生物技术公司、学术界以及监管机构的 RWE 领导和专家
2、国家药品监督管理局药品审批中心,NMPA,《真实世界证据支持药物研发的基本考虑(征求意见稿)》
http://www.cde.org.cn/news.do?method=viewInfoCommon&id=314865
3、NMPA,真实世界证据支持药物研发与审评的指导原则(试行). http://www.nmpa.gov.cn/WS04/CL2138/373175.html (中文版)
如对本文有任何问题,请联系:APAC@Parexel.com
2、精于全球法规 助您研发问鼎!——新冠下全球新药开发申报、临床设计与供应链策略研讨会;
3、冯胜博士解读真实世界数据如何帮助临床试验;
4、李长青博士解读新冠疫情下,全球申报&新药开发战略;


发布者:药时代,转载请首先联系contact@drugtimes.cn获得授权






 为好文打赏 支持药时代 共创新未来!
为好文打赏 支持药时代 共创新未来! 
