浏览量 3434


本文转自综合整理,作者精准药物
点击访问原文链接
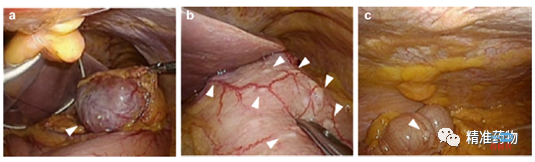
胃肠间质瘤(Gastrointestinal Stromal Tumors,GIST)是胃肠道最常见的间叶源性肿瘤,在生物学行为上可从良性至恶性,免疫组化检测通常表达CD117和DOG1阳性,大多数病例具有c-kit或血小板源性生长因子受体α(platelet derived growth factor receptor alpha,PDGFRA)基因活化突变,少数病例涉及其他分子改变,包括SDHX、BRAF、NF1、K/N-RAS及PIK3CA等基因突变等。
从整个消化道肿瘤的发病情况来看,GIST的发病率仅次于胃癌和结直肠癌,占胃肠道恶性肿瘤的1%-3%。
GIST的年发病率约为10-15/100万,中国每年发病人数约为2-3万例。美国每年新诊患者超过5000例。GIST在不同地理位置的发病率有所不同,在4.3-6.8/百万到19-22/百万之间。
GIST发病的中位年龄在50岁左右。胃部是最常见的原发部位(55%),其次是小肠(30%)和直肠(5%)。极少数情况下,GIST在其他胃肠道部位或胃肠道外的脏器发生。
过去,GIST被分为胃肠道肉瘤、平滑肌肉瘤、平滑肌瘤、神经丛肉瘤、平滑肌母细胞瘤、胃肠自主神经肿瘤(GANTs)或恶性非特异性组织细胞瘤等。
直到1998年,科学家才终于搞清楚,V-KIT原癌基因突变是大多数GIST的驱动因子。后来,首位晚期GIST患者使用ABL/PDGFR/KIT多激酶抑制剂伊马替尼进行了治疗。FDA于2002年2月批准伊马替尼用于晚期GIST患者。
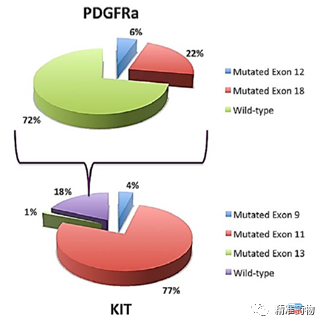
随后研究证实,GIST中最常见的致癌驱动基因为c-KIT和PDGFRA突变,其中c-KIT约占80%,PDGFRA突变约占10%,还有10%的GIST缺少c-KIT或PDGFRA突变,称为野生型GIST。
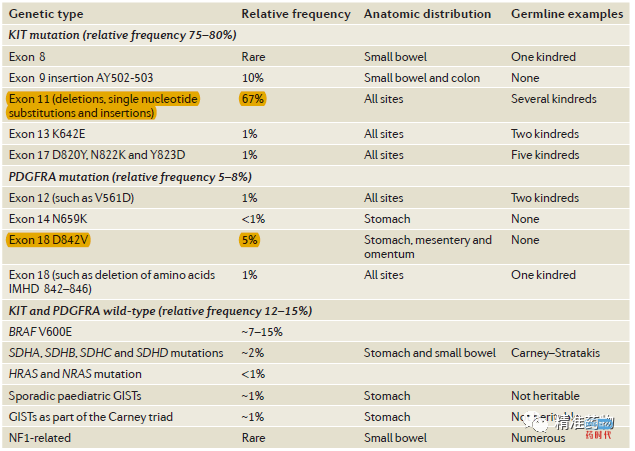
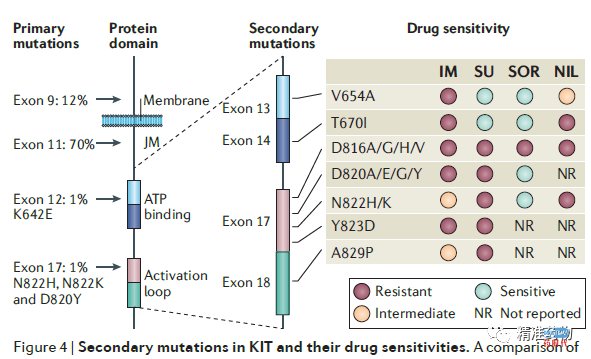
大多数c-KIT突变发生在第11外显子(90%)或第9外显子(8%),较少发生在第13外显子(1%)或第17外显子(1%);PDGFRA突变最常见于第12、14和18外显子中,第18外显子中的D842V突变频率最高(62.6%)。
中国学者的研究结果表明,外显子11突变也是国人最常发生的c-KIT突变,占到66.9%,而在PDGFRA基因突变中最常发生于外显子18和12。与西方人群相比,中国患者的的GIST患者的基因突变位点和突变类型并无显著差异。
野生型GIST被证明与多种基因突变有关。本文仅描述GIST的KIT和PDGFRA突变。
1998年,人们首次报道GISTs中存在激活KIT突变,这是个里程碑式发现。现已证实:约75%的GIST患者中存在KIT激活突变。突变激活可以让GIST细胞非依赖配体的恶性增殖。
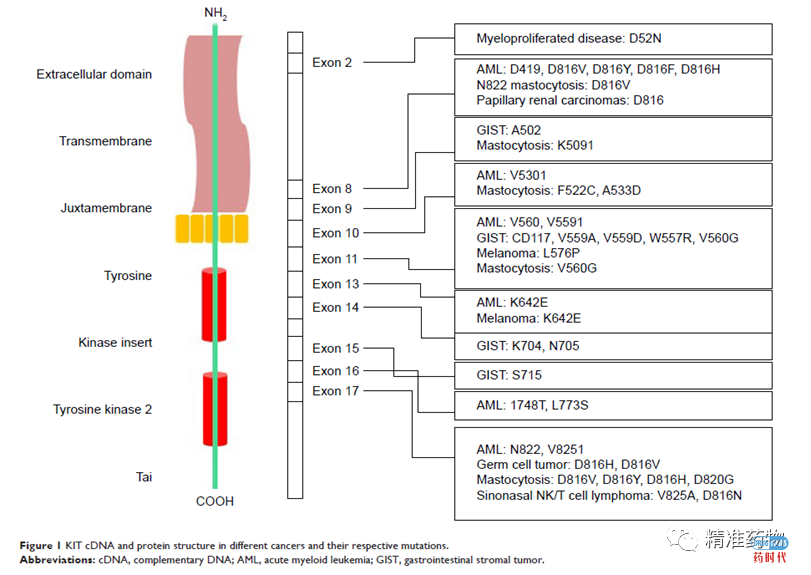
KIT是一种跨膜的III型酪氨酸激酶受体,其配体为干细胞因子(SCF)。正常状态下,SCF配体结合KIT后,诱导其二聚并激活下游信号通路,如JAK–STAT3、PI3K–AKT–mTOR和RAS–MAPK等。
KIT激活突变发现后2年,伊马替尼被确证为有效的KIT抑制剂。又1年后,伊马替尼被用于治疗1位转移性GIST患者,并取得良好疗效。随后,使用伊马替尼治疗晚期GIST患者的大型队列临床试验取得了显著成功。从此,GIST的临床治疗迎来靶向治疗时代,并成为精准医疗的成功范例。
约2/3的GIST患者存在KIT基因11号外显子激活突变。这个位置的突变消除了KIT膜旁结构域(JM)的自抑制功能,从而导致了KIT持续激活。在各种形式的突变中,缺失突变是最常见的类型,其次是点突变。
一般来说,由于外显子11突变引起的KIT构象变化会破坏受体的自抑制结构域,并允许持续的激酶激活。绝大多数(大于80%)外显子突变的GIST位于胃部。密码子557或558的缺失是最常见的突变,这些突变被证明与在欧洲GIST患者的预后较差有关。而日本Yamaguchi等发现KIT基因11号外显子突变与肝转移的发生有关,并与伊马替尼治疗前糟糕的临床预后相关。
KIT基因9号外显子突变占GISTs的8-10%,其中95%是细胞外域中502和503位密码子的重复。由此产生的构象变化可以模拟SCF的结合,从而导致二聚和持续性激活。476位密码子突变的报道很少。
KIT基因9号外显子突变比11号外显子突变与GIST耐药更相关。KIT基因9号外显子突变更容易发生在小肠或大肠,而胃部GIST只有2%发生这个位置的突变。
体外研究表明,KIT基因9号外显子突变降低了伊马替尼的敏感性。临床试验也证明,在不可切除的转移性GIST中,KIT基因9号外显子突变是总生存率和无进展生存率(PFS)的不利标志。然而,这种耐药性可以通过使用更高剂量的伊马替尼(800毫克vs 400毫克)来克服,获得的应答率几乎可与携带试剂盒第11外显子突变的肿瘤患者相媲美。
KIT基因13号外显子突变如1945A>G等发生几率非常罕见,大约在1%左右。携带该突变的GIST通常在胃部,表现为梭形细胞形态。该位置突变的功能后果尚不清楚;一些报告表明它们对伊马替尼敏感;也有报道发现伊马替尼和舒尼替尼治疗失败患者中存在13外显子突变。
KIT基因17号外显子定位于激活环(Activation loop),该位置的突变能够维持KIT的活性构象,但突变几率较低。其突变大多涉及822位密码子,其中2487T>A替代突变是常见的。虽然该突变对伊马替尼的敏感性较低,但对瑞格非尼(regorafenib)敏感。
PDGFRA是GISTs中第二常见的突变癌基因;其功能与KIT存在重叠,因此PDGFRA和KIT突变在GIST中是相互排斥的。
大多数PDGFRA突变的GIST发生在胃部,通常具有上皮样或混合上皮样和梭形细胞组织学,通常伴有粘液样基质改变。
虽然下游的激活途径与KIT突变相同,但PDGFRA突变的GIST往往具有较低的复发风险。
法国的一项研究显示,KIT和PDGFRA突变分别在71%和15%的GIST患者中被检测到。然而,在转移性GIST中,只有2.1%的患者表现出PDGFRA突变,而KIT突变的患者中只有82.8%出现PDGFRA突变。
GIST中的大多数PDGFRA突变发生在18号外显子,其能稳定激酶激活环:
-
约70%的PDGFRA突变为D842V突变,该突变介导伊马替尼原发性耐药。最近开发的PDGFRA抑制剂crenolanib能够克服D842V突变耐药。
-
第二个最常见的是842到845密码子的缺失,这种突变对伊马替尼敏感。
PDGFRA基因12号外显子突变是GIST中第二常见,被认为占GIST的1-2%。外显子12突变通常表现为缺失而非重复,1821T>A是共同位点,导致Val561Asp在蛋白质水平上发生替换。
PDGFRA膜旁结构域被认为介导了一种自身抑制功能,而这个抑制结构域的突变导致了过度激活。
PDGFRA突变很少发生在第14号外显子,该突变经常发生在密码子659处。
外显子14与外显子12相近;因此,它也可能参与膜旁结构域的自我抑制功能,并表现出相似的表型。
50%以上的原发性、局限性和可切除性GIST可单独通过手术治疗。但是大约25%的患者在诊断时就已经发生转移,约40%的患者在初次外科手术后复发。
长时间内,GIST的临床治疗效果不佳。常规化疗的有效率<5%,晚期患者的中位生存期约为18个月。直到2000年,多激酶抑制剂伊马替尼用于GIST的治疗,这种状况才得以改善。
KIT受体通常处于活性构象和非活性构象之间的平衡状态。非活性构象受到由膜旁结构域所赋予的空间位阻的支持,这种位阻阻止了活化环假设激酶活化所需的构象。在这种非活性状态下,伊马替尼与铰链区的氨基酸Cys673、近端激酶结构域中的Glu640以及近端和远端激酶结构域之间的DFG基序中的Asp810和Phe811结合;伊马替尼这种结合能够稳定KIT激酶处于失活构象状态。
伊马替尼首次用于临床治疗一名50岁的女性转移性GIST,其疗效显著。大规模的国际临床试验表明,伊马替尼在70-85%的晚期KIT阳性GIST患者中实现了疾病控制,中位无进展生存期为20-24个月。
目前,伊马替尼是GIST的一线治疗药物,接受伊马替尼治疗的晚期GIST患者的中位生存期为5年左右,34%的患者存活时间超过9年。
最近,伊马替尼也被证明可以降低治愈性手术后复发的风险。
虽然伊马替尼的应用给GIST临床治疗带来突破性进展,但并不是所有GIST患者都有效,而且大多数接受伊马替尼敏感的GIST患者大多会产生耐药性并最终恶性进展。
对KIT和PDGFRA抑制剂(如伊马替尼)治疗的耐药性可分为两类:原发性和继发性。
原发性耐药:大约10%的GIST患者有原发性耐药。KIT外显子11、KIT外显子9和野生型GISTs对伊马替尼的原发耐药率分别为5%、16%和23%。
尽管在没有伊马替尼治疗的情况下,KIT第11外显子突变GISTs的临床预后较差,但该突变在体外对伊马替尼高度敏感,其半数最大抑制浓度(IC50)<100nm;而KIT第9外显子突变和KIT野生型GIST对伊马替尼的敏感性较低(约1000 nM)153。因此,伊马替尼在外显子9突变患者中的剂量不足可能是造成明显耐药性的原因。
根据体外数据,GIST中最常见的PDGFRA突变D842V,对伊马替尼具有很强的抗性。这种突变有利于激酶结构域的活性构象,因此不利于伊马替尼的结合。
在伊马替尼最初受益后,绝大多数患者最终会出现疾病进展或继发性耐药。
与主要在外显子9和11编码的KIT激活突变不同,激发突变集中在KIT激酶结构域的两个区域,这是伊马替尼靶向的结构域:
-
一种是ATP结合袋,由外显子13和14编码,其突变直接干扰药物结合;
-
第二个是激活环,突变可以稳定KIT的活性构象,从而阻碍药物相互作用。
-
几乎所有的外显子17或18 KIT继发突变也可以作为原发激活突变,从而潜在地增加激酶活性。
在GIST中也观察到PDGFRA突变耐药,最常见的是获得性D842V突变(激活环)。
更令人警醒的是,不同病变之间,甚至同一病变的不同区域内,存在着相当大的异质性耐药。有报道说
-
-
在同一个病人的多个肿瘤中有多达7个不同的激发耐药突变。
这种耐药性的异质性在很大程度上影响了一线伊马替尼治疗后挽救TKI疗法的疗效,因为耐药少数克隆的多样性阻止了任何特定TKI对GIST细胞的系统性根除。
尽管KIT的继发突变是获得性对伊马替尼治疗产生耐药性的最常见原因,但还有其他多种因素参与其中,如KIT和PKC表达下调或丢失、IGF1R的过度表达、粘着斑激酶(FAK)、AXL过度表达等。
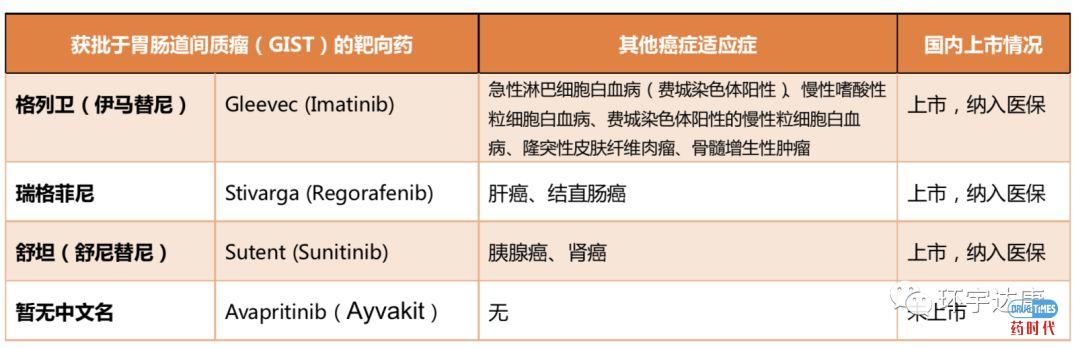
舒尼替尼(Sunitinib)和瑞戈非尼(regorafenib)对伊马替尼耐药的GIST具有活性,在伊马替尼失效后被用作二线和三线治疗药物。不幸的是,由于耐药克隆的异质性等原因,药物有效能够维持的时间比较短。
舒尼替尼(Sunitinib)对KIT外显子13和14的改变(例如p.V654A或p.T670I)是有效的,因为它的结合不受突变的阻碍。然而,由KIT外显子17和18编码的受体激活环(A-loop)的继发突变对伊马替尼和舒尼替尼都有耐药性。
瑞戈非尼(regorafenib)用于治疗GIST在伊马替尼和舒尼替尼失败后患者。尽管它已经证明对A环中的某些突变具有活性,但由于不能抑制p.D816V突变,因此其临床益处相当有限,并且在一年内会再次发生不良进展。
Avapritinib(BLU-285)是一种口服的、强效选择性的KIT和PDGFRα抑制剂。Avapritinib在KIT和PDGFRA突变的胃肠道间质瘤(GIST)中显示了广泛的抑制作用,包括PDGFRA基因 D842V 突变和其他原发或继发耐药突变;但仍对多个KIT及PDGFRA突变无效。
2020年5月16日,再鼎医药合作伙伴Deciphera制药公司宣布,FDA提前3个月批准其广谱KIT和PDGFRα激酶抑制剂Ripretinib(Qinlock,DCC-2618)上市,用于四线治疗晚期胃肠道间质瘤(GIST);Ripretinib适用于先前接受过3种或3种以上激酶抑制剂治疗的成人患者,包括:伊马替尼[imatinib]、舒尼替尼[sunitinib]、瑞戈非尼[regorafenib])等。
因此,Ripretinib(DCC2618)的上市进一步解决了GIST的临床耐药问题。
但所有靶向治疗药物均会最终产生耐药,因此GIST的治疗仍面临持续不断的挑战,我们也需要开发更加安全有效并且克服耐药的药物。
内容仅供感兴趣的个人谨慎参考,非商用,非医用、非投资用。版权归作者。衷心感谢!
版权声明:文中图片取自网络,根据CC0协议使用,版权归拥有者。
任何问题,请与我们联系。衷心感谢!


 点击这里,欣赏更多有价值的医药资讯!
点击这里,欣赏更多有价值的医药资讯!
本文转载自综合整理,本文观点不代表药时代DrugTimes立场。


 点击这里,欣赏更多有价值的医药资讯!
点击这里,欣赏更多有价值的医药资讯!


 为好文打赏 支持药时代 共创新未来!
为好文打赏 支持药时代 共创新未来! 
