
HIF的作用机制

The 2019 Nobel Prize in Physiology or Medicine is awarded jointly to William G. Kaelin Jr, Sir Peter J. Ratcliffe and Gregg L. Semenza “for their discoveries of how cells sense and adapt to oxygen availability.”
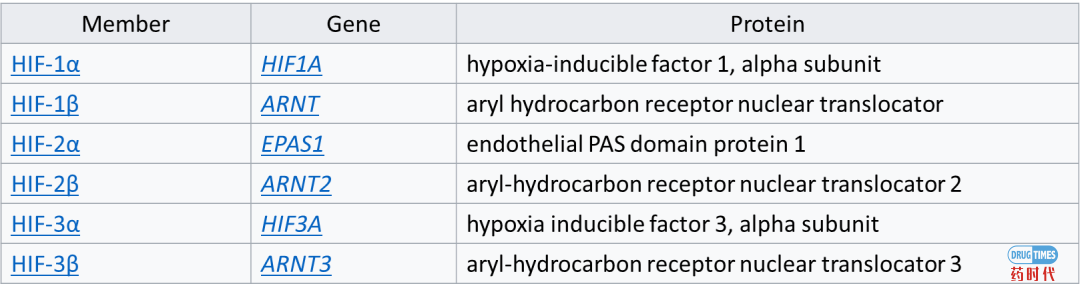
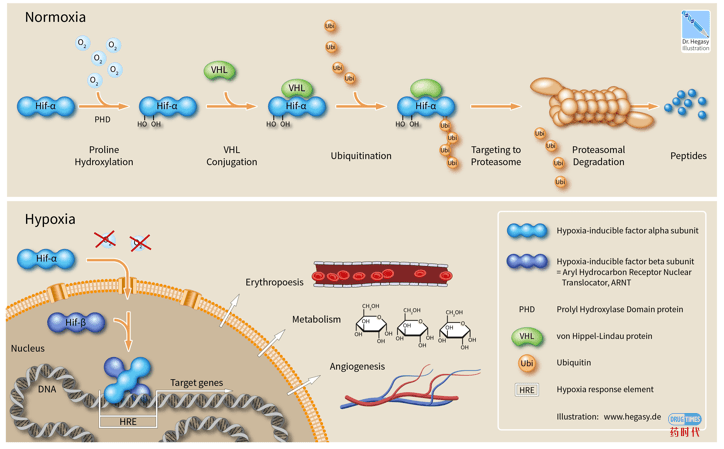
HIF-2α别构抑制剂的发现


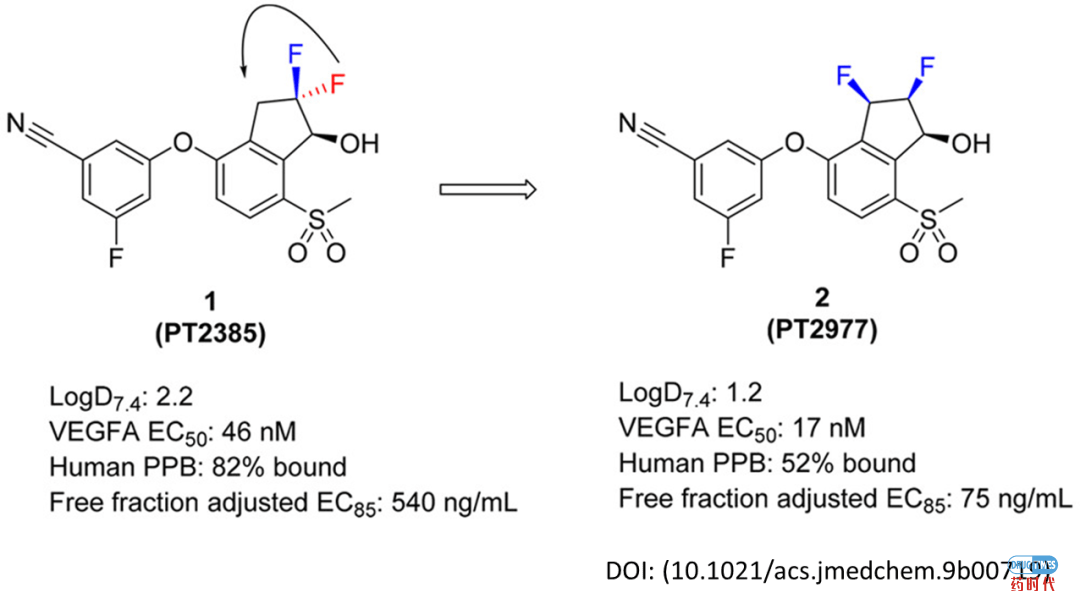
HIF-2α别构抑制剂的改进
默沙东收购Peloton
HIF-2α最新临床进展及研发方向
小结
参考文献:
3、A Small-Molecule Antagonist of HIF2α Is Efficacious in Preclinical Models of Renal Cell Carcinoma. Eli M. Wallace, James P. Rizzi, Guangzhou Han, et al. Cancer Res. 2016 Sep 15;76(18):5491-500. doi: 10.1158/0008-5472.CAN-16-0473.
4、3-[(1S,2S,3R)-2,3-Difluoro-1-hydroxy-7-methylsulfonylindan-4-yl]oxy-5-fluorobenzonitrile (PT2977), a Hypoxia-Inducible Factor 2α (HIF-2α) Inhibitor for the Treatment of Clear Cell Renal Cell Carcinoma. Xu R, et al. J Med Chem. 2019 Aug 8;62(15):6876-6893.
5、Allosteric inhibition of HIF-2α as a novel therapy for clear cell renal cell carcinoma. Yu Y, Yu Q, Zhang X. Drug Discov Today. 2019 Dec;24(12):2332-2340. doi: 10.1016/j.drudis.2019.09.008.
6、Hypoxia signaling in human diseases and therapeutic targets. Jae W. Lee et al. Experimental & Molecular Medicine. 2019, volume 51, pages1–13.
7、HIF-2 Complex Dissociation, Target Inhibition, and Acquired Resistance with PT2385, a First-in-Class HIF-2 Inhibitor, in Patients with Clear Cell Renal Cell Carcinoma. Courtney KD, Ma Y, Diaz de Leon et al., Clin Cancer Res. 2020 Feb 15;26(4):793-803. doi: 10.1158/1078-0432.CCR-19-1459.


发布者:药时代,转载请首先联系contact@drugtimes.cn获得授权

 为好文打赏 支持药时代 共创新未来!
为好文打赏 支持药时代 共创新未来! 
