
第二届中国新药CMC高峰论坛即将开幕!点击下图查看参会指南 ↓

一文了解以下几个要点:
-
瑞基奥仑赛(Relma-cel)获批上市;这是中国首款按1类生物制品获批的CAR-T产品;
-
免疫细胞治疗CAR-T作用机理是什么?
-
CAR-T是怎么炼成的?
-
CD19 CAR-T治疗效果如何?
-
CAR-T治疗会遇到什么问题?有什么解决途径?
1一款CAR-T新产品在中国获批上市
9月3日,一款叫做瑞基奥仑赛(Relma-cel)的抗癌药物获得上市批准,并已获得药品注册证书。这个药物,不是小分子化学药物,也不是大分子蛋白药物,而是一种叫做CAR-T的细胞药物,属于免疫细胞治疗,是一种“活的药物”。
说到CAR-T,大家也许会听说过艾美丽(Emily Whitehead )的抗癌经历。
2010年,当时只有5岁大的艾美丽被诊断为白血病。艾美丽得的这种白血病(acute lymphoblastic leukemia ,ALL),本来相对来说是比较好治的,在美国85%-90%都可以被治愈。但是,艾美丽属于那不太幸运的10%:两轮化疗后,因为腿部出现组织坏死,差点儿被截肢;在治疗一年多后,病情复发,再次接受化疗之后,病情也没有缓解,医生已建议进行临终关怀了。
但是艾美丽的父母没有放弃,让她参加了美国宾夕法尼亚大学医学院的一项新的临床试验。当时是2012,艾美丽7岁。
结果呢?艾美丽如今16岁了,身体内早已检测不到癌细胞,而且一直都检测不到癌细胞。只要5年内都没有复发,就达到了临床治愈的标准,所以,艾美丽的癌症,可以说已经被治愈了。

图: 艾美丽于2021。图片来自EmilyWhitehead基金会网站
救了艾美丽的,就是CAR-T,全名叫做“嵌合抗原受体T细胞”免疫治疗。在2017,第一款CAR-T药物在美国获得FDA批准。今年,中国终于有了正式获批的CAR-T产品。
那么,CAR-T到底是一个什么样的药物呢?
2CAR-T原理:突破性技术是怎么做到的?
CAR-T是细胞免疫治疗,药物是源自患者身体体内的T细胞。
T细胞是免疫细胞的一种,可以抗击入侵的病毒,也可以杀灭癌变的细胞。所以,病毒、癌细胞,都是T细胞的敌人。
要打击敌人,首先是要能够识别敌人。T细胞之所以能识别敌人,是因为T细胞表面特殊的T细胞受体(TCR)。

这个T细胞受体,就是感应是否有敌人的“雷达”。T细胞有一种机制,可以随机地产生成千上万种“雷达”,但是,每一个T细胞,只有一种“雷达”。
以病毒为例,当病毒入侵后,免疫系统能够捕获病毒上的抗原信息,再找到能够特异性识别这种抗原的T细胞,然后将其大量扩增。当病毒再次入侵时,就会有大量的T细胞对病毒发起攻击。
接种疫苗所达到的效果,就是激活免疫保护——不只是产生抗病毒的抗体,也可能激活产生大量的抗病毒特异性T细胞。
对于癌细胞,情况就不太乐观。癌细胞也是源自自体的细胞,本来隐蔽性就很好,不容易识别,虽然在成千上万的T细胞中,总能找到几个可以识别癌细胞上的特殊抗原,但是因为数量太少,基本没有抗癌效果。
CAR-T怎么“炼制”呢?这种治疗,是先收集患者的T细胞,然后强制性地在T细胞表面表达一个能识别癌细胞的“感应器”,也就是装上了一个人造的T细胞受体。这样一个人造受体,叫做“嵌合抗原受体”(CAR)。
CAR就插在T细胞的细胞膜上,伸展在细胞外面的,是能识别癌细胞的抗体分子,一旦感应到了癌细胞,就会通过内部的功能区域激活T细胞,对癌细胞造成杀伤。
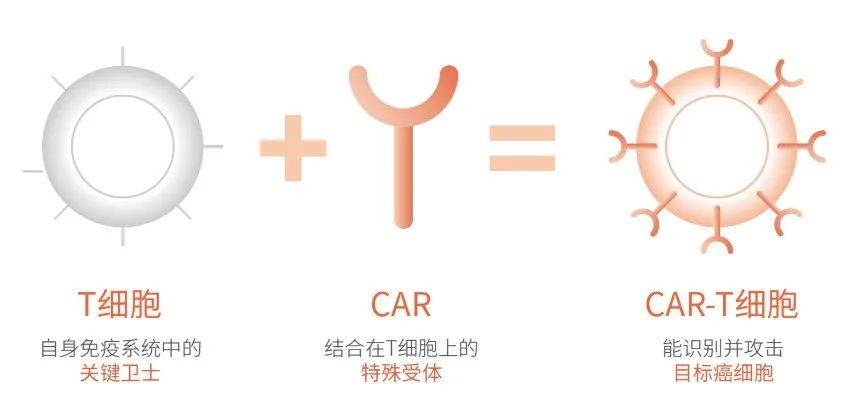
(图片来源于药明巨诺,版权归其所有)
瑞基奥仑赛的CAR,外部是一个识别CD-19的抗体,所以属于CD-19 CAR-T。在瑞基奥仑赛CAR上,有一段4-1BB共刺激域,处于细胞内。并不是所有CAR-T都有这个4-1BB共刺激域,有了这段4-1BB共刺激域,可以让CAR-T细胞得到更持久的激活,从而提高CAR-T的疗效,也能增加安全性[1, 2]。
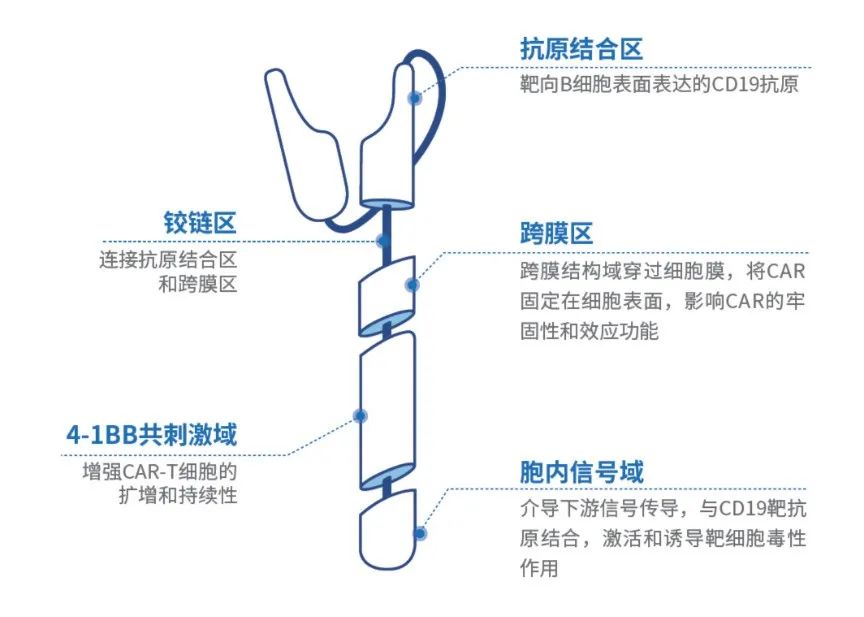
图:瑞基奥仑赛(CD19 CAR-T)结构示意图。
(图片来源于药明巨诺,版权归其所有)
3CAR-T的临床试验数据如何?
CAR-T是一种细胞免疫治疗,要制备CAR-T细胞,需要先将患者外周血单核细胞分离出来,作为CAR-T的原材料。由于中国法律法规不允许将采集的患者外周血送到国外,因此在国内获批的CAR-T疗法,必须要具有一套完整的本土化生产制备工艺。俗话说“橘生淮南则为橘、橘生淮北则为枳”,国内获批的CAR-T治疗产品效果如何,还需要看在国内进行的临床试验数据。
瑞基奥仑赛在中国进行生产,也在中国进行了一项前瞻性、单臂、多中心、关键性研究(RELIANCE)[3],治疗的是复发/难治性大B细胞淋巴瘤(r/r LBCL)患者。RELIANCE研究是瑞基奥仑赛在中国开展的CAR-T注册临床研究,也是目前中国最大规模的CAR-T治疗R/R LBCL的注册临床研究。
值得一提的是,RELIANCE研究更贴合中国人群情况,是在中国临床环境下、通过标准注册临床路径得出的高质量研究结果,研究的结果也成为关键的有效性数据,作为瑞基奥仑赛在中国上市申请的依据,提交给药监部门审批。
该临床试验所入组的患者中,总共有59例患者接受了瑞基奥仑赛CAR-T治疗,有58例患者可评估治疗有效性。临床试验的主要终点为治疗3个月后的客观缓解率(objective response rate,ORR)。
总体上,有75.9%接受治疗的患者都出现了客观缓解,其中完全缓解率为51.7%。部分缓解率为24.1%。在治疗后3个月时,客观缓解率为60.3% (95% CI,46.6~73.0)。这个数据表明该临床试验达到了主要终点。
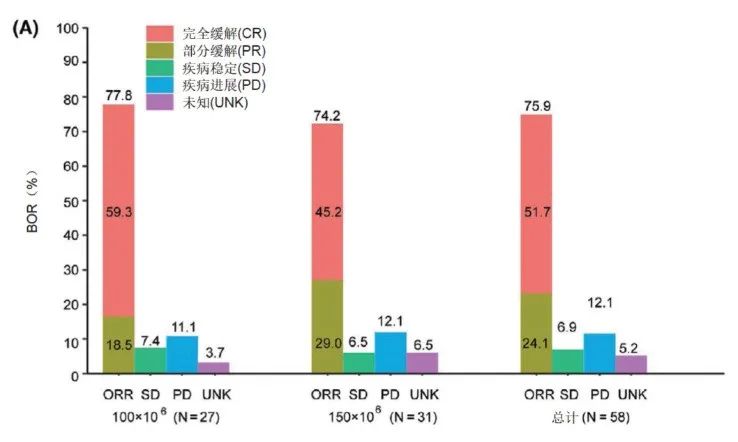
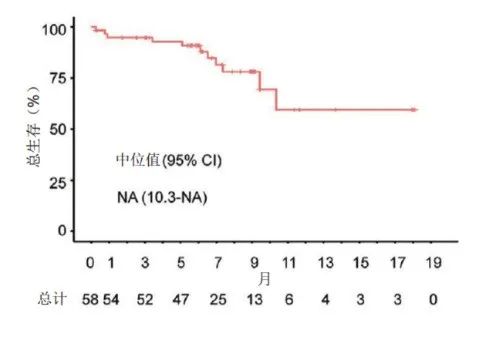
该研究的中位随访时间为8.9个月,中位PFS和DOR分别为7.0个月(95% CI,
5.5~NA)和8.0个月(95% CI,6.0~NA),尚未达到中位OS。
4CAR-T目前可用于哪些肿瘤的治疗?
在我国,淋巴瘤是一种常见的恶性肿瘤,而且发病人数增长迅速,主要发生于成年人,70-74岁是发病高峰。在所发生的淋巴瘤中,90%都是非霍奇金淋巴瘤,只有10%是霍奇金淋巴瘤[4]。
瑞基奥仑赛目前批准的适应证,是经过二线或以上系统性治疗后成人患者的复发或难治性大B细胞淋巴瘤(r/r LBCL)。
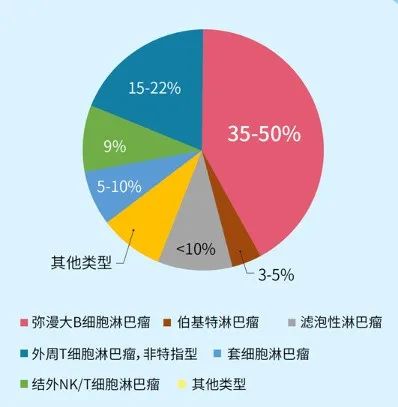
图:非霍奇金淋巴瘤的种类。弥漫型大B细胞淋巴瘤(DLBCL)是一种最常见的非霍奇金淋巴瘤,占比为35-50%。
在初诊检查出DLBCL之后,目前一线标准治疗方案是化疗,如果复发,条件允许的话可能还需要进行自体造血干细胞移植(ASCT)。但即便进行了ASCT,有50%的患者还是会复发。
由于大B细胞淋巴瘤的肿瘤细胞表面有CD-19,靶向CD-19的瑞基奥仑赛就可以有效地杀死肿瘤细胞。除了大B细胞淋巴瘤,其他的一些恶性肿瘤,如急性淋巴细胞白血病(ALL)、套细胞淋巴瘤(MCL),肿瘤细胞表面也有CD-19靶点,所以在国外也有获批CD-19 CAR-T治疗。目前国际上获得批准的CAR-T,还有另外一个靶点:BCMA。BCMA CAR-T用于治疗复发、难治型多发性骨髓瘤。
虽然靶向CD-19的CAR-T对于其他肿瘤也有治疗潜力,但想要正式在临床上获得应用,仍然需要针对不同的适应症做临床试验,这些规定是严谨和必要的,但CAR-T的应用前景仍然被许多人看好。
5CAR-T常见副作用都有些什么?
CAR-T常见的副作用,有细胞因子释放综合征(CRS,即常说的细胞因子风暴)和神经毒性。在瑞基奥仑赛的临床试验中,任何级别CRS和重度CRS的发生率分别为47.5%和5.1%,而任何级别神经毒性和重度神经毒性事件发生率分别为20.3%和3.4%。
细胞因子风暴和神经毒性通常是可以控制的,有效的药物,是托珠单抗(白细胞介素IL-6受体抗体)。
1999年,一名患者在参加宾夕法尼亚大学的基因治疗临床试验时,因为出现了细胞因子风暴而去世。这名18岁的患者在注射了携带正常OTC基因的腺病毒载体,在几小时后体征出现反常,当夜高烧,次日凌晨神志不清,于4天之后死亡。
这个临床试验的失败,让全球的基因治疗临床研究挫折了将近20年。这个失败的临床试验跟CAR-T没有关系,但是却孕育了CAR-T的成功。在基因治疗的患者去世后,宾夕法尼亚大学的专家们意识到了一个问题:如果没有解决细胞因子风暴的好办法,很多治疗将无法顺利进行。通过研究发现,发生细胞因子风暴时,患者血液中IL-6浓度较高,而托珠单抗有很好的抗细胞因子风暴的效果。
所以,当CAR-T临床试验在宾夕法尼亚大学开展时,又再次出现了细胞因子风暴,但这次临床试验没有在风暴中翻船,通过使用托珠单抗,患者的状况获得了稳定,避免了严重后果的发生。除了托珠单抗之外,对于一些副作用比较严重的患者,也可辅助使用糖皮质激素来进行控制。
瑞基奥仑赛的临床试验显示,主要副作用其实控制得都比较好,低剂量组(注射1亿个CAR-T细胞)并没有出现严重的细胞因子风暴和神经毒性,同时,低剂量组的ORR数据也不比高剂量组差。
与其他CAR-T临床试验数据相比,研究者认为瑞基奥仑赛的有效性和安全性与其他国际上批准的同类产品相似,在安全性数据方面,瑞基奥仑赛比CD28 CAR-T产品有优势[3]。
6结语
在与癌症的斗争中,人类很长一段时期都处在下风,但随着科学的发展,人们对于癌症治疗的探索也从未停止。对于需要治疗的患者来说,CAR-T正从一个“江湖传说”转变为能够“治病救人”的产品,希望在未来,CAR-T能够拯救更多有需要的患者,让更多人获益。
参考文献:
1. Zhao,X., et al., Efficacy and Safety of CD28- or 4-1BB- Based CD19 CAR-T Cells in B Cell Acute Lymphoblastic Leukemia. Molecular Therapy – Oncolytics, 2020. 18:p. 272-281.
2. Lu, P., et al., Which is better in CD19 CAR-T treatment of r/r B-ALL, CD28 or 4-1BB? A parallel trial under the same manufacturing process. Journal of Clinical Oncology, 2018. 36(15_suppl): p.3041-3041.
3. Ying, Z., et al., Relmacabtagene autoleucel (relma‐cel) CD19 CAR‐T therapy for adults with heavily pretreated relapsed/ refractory large B‐cell lymphoma in China. Cancer medicine, 2021. 10(3): p.999-1011.
4. Liu, W., et al., Burden of lymphoma in China, 2006–2016: an analysis of the Global Burdenof Disease Study 2016. Journal of Hematology & Oncology, 2019. 12(1): p. 115.
(作者:张洪涛,笔名“一节生姜”。宾夕法尼亚大学医学院病理及实验医药系研究副教授,研究领域:癌症的靶向治疗以及免疫治疗。著有科普读物:《吃什么呢?——舌尖上的思考》,《如果舌尖能思考》。可以谈最前沿的医学研究,也可以讲最通俗的故事。)

版权声明/免责声明
本文为授权转载文章,版权归拥有者。
仅供感兴趣的个人谨慎参考,非商用,非医用、非投资用。
欢迎朋友们批评指正!衷心感谢!
文中图片、视频为授权正版作品,或来自微信公共图片库,或取自网络
根据CC0协议使用,版权归拥有者。
任何问题,请与我们联系(电话:13651980212。微信:27674131)。衷心感谢!

推荐阅读




11月11日,一个非常特别的日子!
我们在上海张江,一个非常特别的地方,
探讨一个非常特别的话题!
我们不见不散!
 点击这里,欣赏更多精彩内容!
点击这里,欣赏更多精彩内容!
本篇文章来源于微信公众号:药时代
发布者:药时代,转载请首先联系contact@drugtimes.cn获得授权

 为好文打赏 支持药时代 共创新未来!
为好文打赏 支持药时代 共创新未来! 