
欢迎参加2020中国NASH大会!

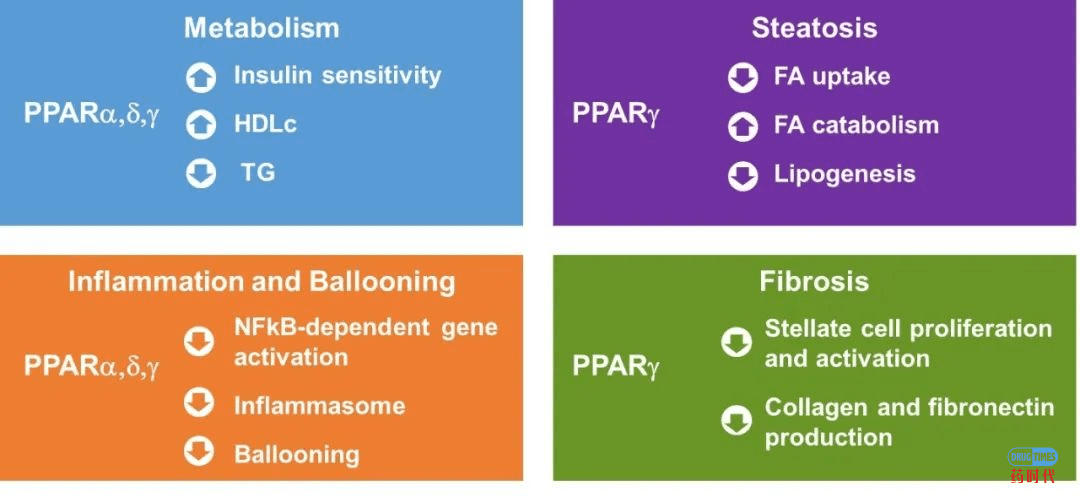
有效性
-
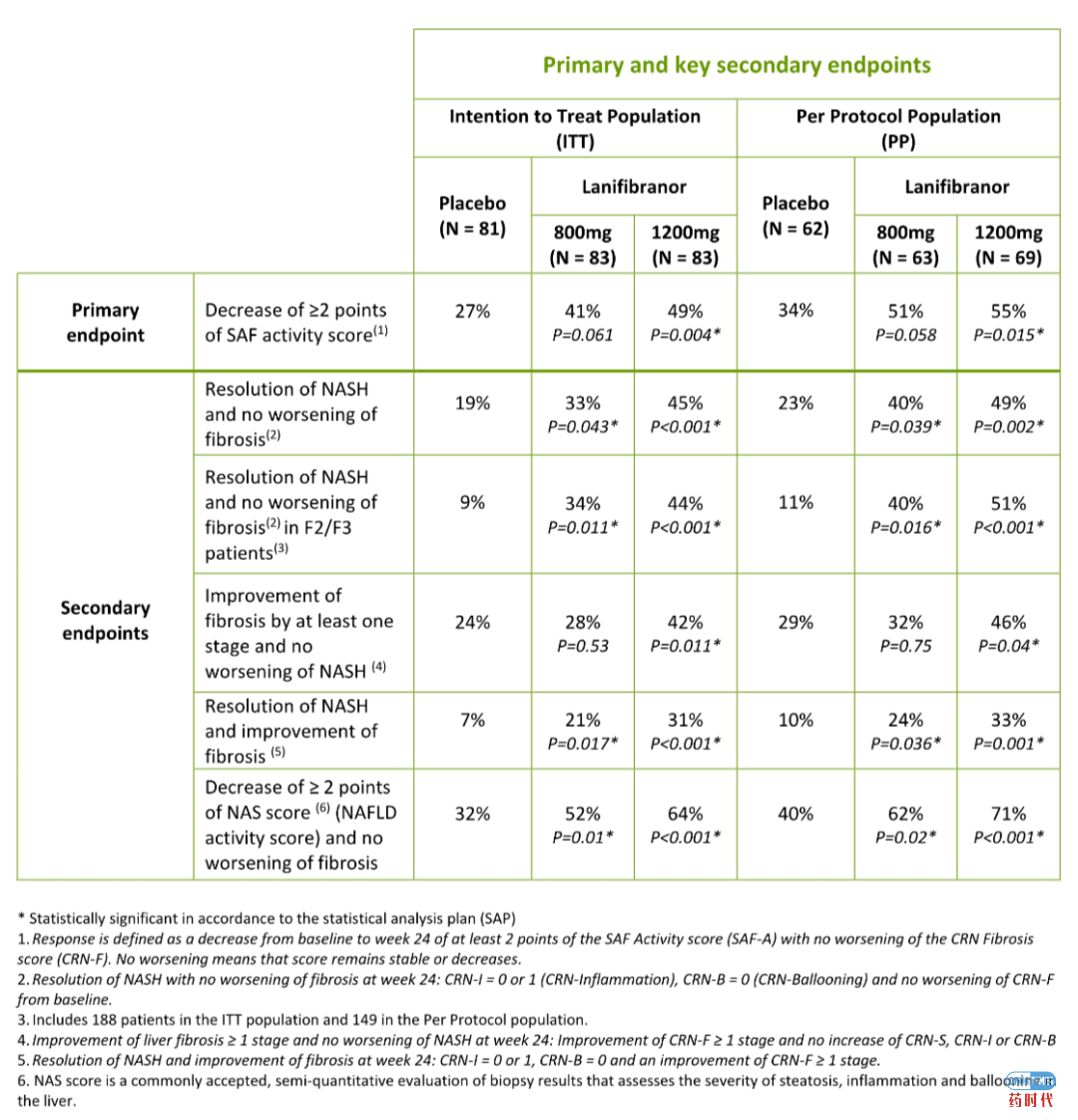
两个剂量组(800mg/d和1200mg/d)的NASH均无纤维化恶化 -
在1200mg/d的剂量组中,纤维化至少改善了1个阶段,且NASH没有恶化 -
两个剂量组(800mg/d和1200mg/d)的NASH缓解和纤维化改善
-
2型糖尿病患者胰岛素、空腹血糖和糖化血红蛋白(HB1AC)降低 -
甘油三酸酯减少 -
高密度脂蛋白胆固醇(HDL)升高 -
肝酶(ALT,AST和GGT)降低
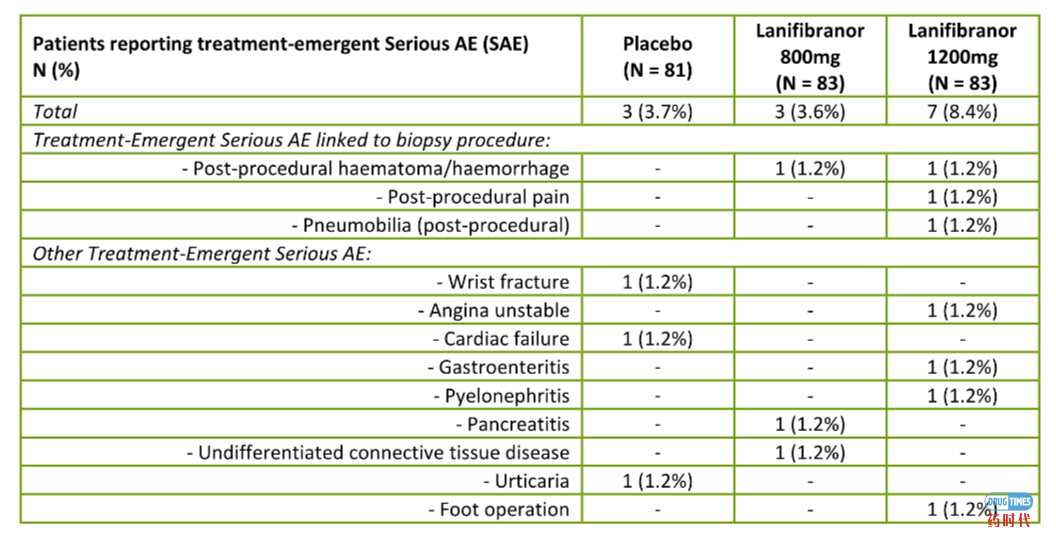
安全性
参考资料:
3、原创 | FDA推迟奥贝胆酸专家组会议
4、http://inventivapharma.com/2020/06/inventivas-lanifibranor-meets-the-primary-and-key-secondary-endpoints-in-the-phase-iib-native-clinical-trial-in-non-alcoholic-steatohepatitis-nash/
5、https://clinicaltrials.gov/ct2/show/NCT03008070?cond=NASH&spons=Inventiva&draw=2&rank=1
Fiona Yu专栏 | 主攻糖尿病的诺和诺德,能否靠GLP-1通杀全场?

发布者:药时代,转载请首先联系contact@drugtimes.cn获得授权


 为好文打赏 支持药时代 共创新未来!
为好文打赏 支持药时代 共创新未来! 





