作为投资人,我们在临床前新药项目中经常看到hERG的数据,不知道大家是怎么看待的?今天我们就掰开了揉碎了仔细来品品。
据文献统计[1],抗肿瘤药物治疗的心脏毒性主要包括9方面:心功能不全与心力衰竭、冠心病、心脏瓣膜病、心律失常(尤其是QT间期延长)、高血压、血栓栓塞性疾病、周围血管病和卒中、肺动脉高压及心包并发症。其中,QT间期延长的副作用已经成为威胁公众用药安全的重要问题,也是目前药监部门和新药研发公司广泛关注的药物心脏安全性问题。
第一部分:药物的心脏安全性数据
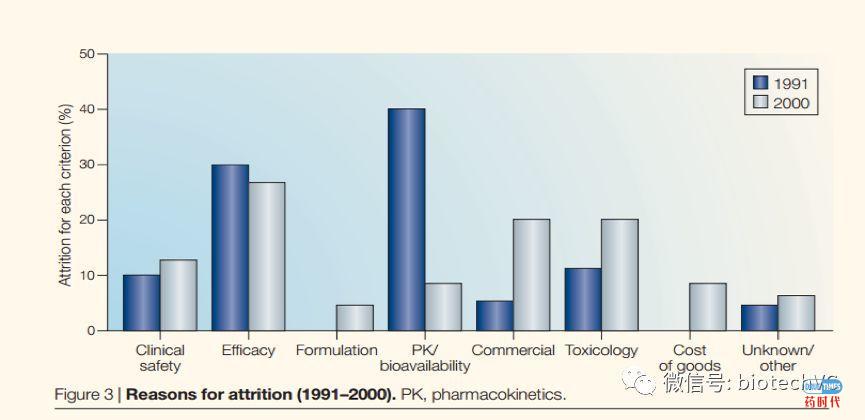
首先,我们来看一张图,看过我们上期文章的读者,肯定会觉得好眼熟……没错,就是那张图,这是Kola于2004年发表的《Can the pharmaceutical industry reduce attrition rates?》。这篇文章统计了阿斯利康,BMS,诺华,辉瑞等欧美前10大的药企在1991年到2000间进入临床阶段的管线的开发情况。其中,因安全性而导致药物研发失败的比重是Toxicology(21%)+Clinical safety(12%)=33% of all failures.
再来看一张图,这是PB Watkins于2011年发表的《Drug Safety Sciences and the Bottleneck in Drug Development》。这篇文章指出导致临床试验失败和已准药物撤市主要是与心血管系统和肝脏有关,其中最易导致撤市的心血管不良事件是可能致命的心律失常,即众所周知的尖端扭转性室性心动过速(TdP),现在可以通过在1期临床试验中监测心电图QT间期来识别。
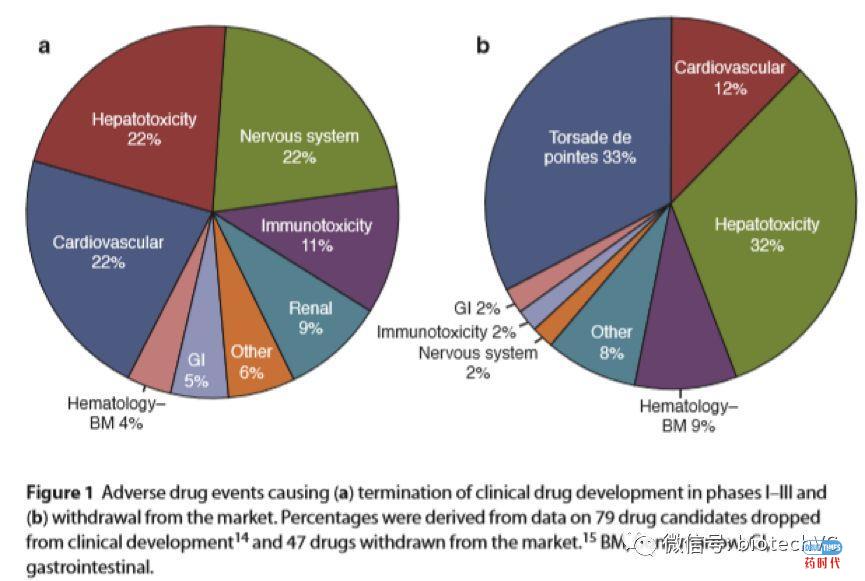
在临床试验I-III期失败的79个药物中,心血管系统占比22%,肝毒性占比22%,中枢神经系统占比22%;
在FDA批准后撤市的47个药物中,TdP占比33%,其他心血管系统占比12%,肝毒性占比32%。
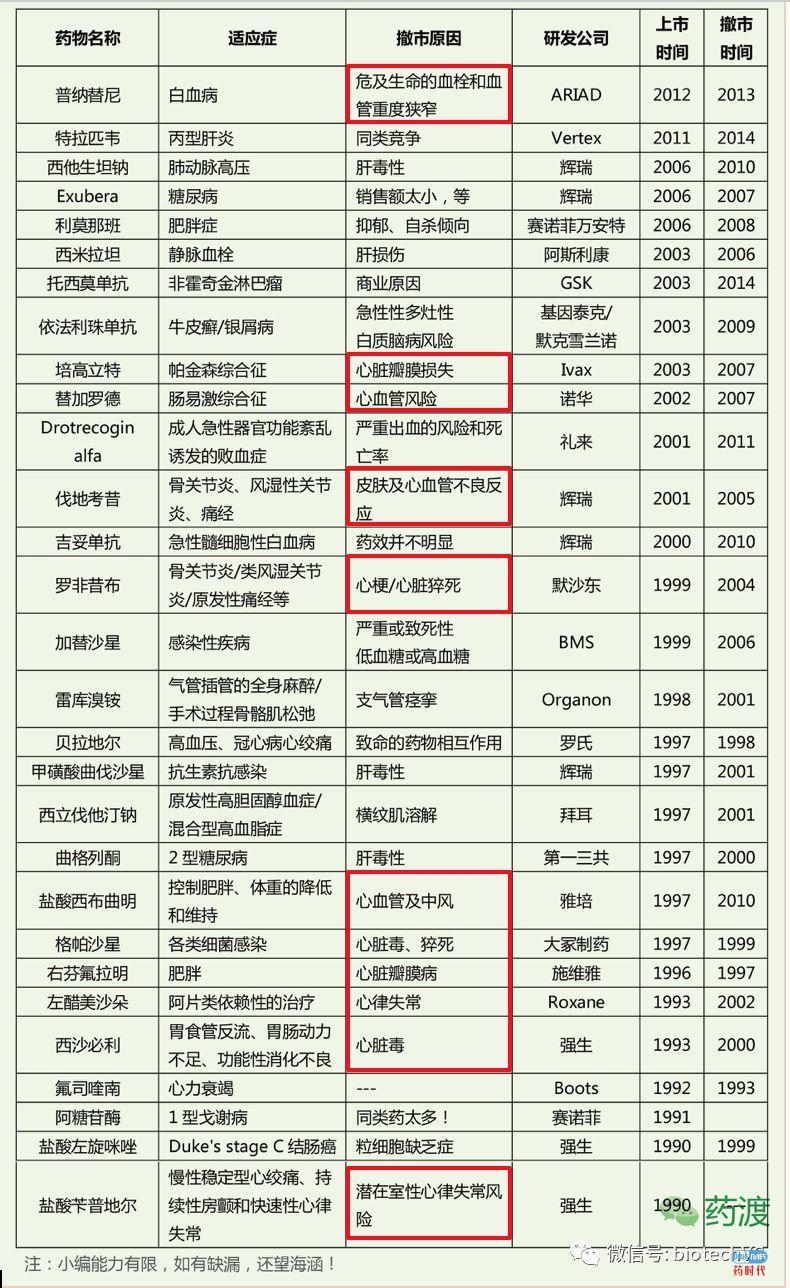
再来看一张转自药渡的90年代后撤市的药物列表,其中好多药物都出自制药豪门,他们往往都具备顶尖的研发团队和充足的研发经费,但尽管如此,仍避免不了药物上市后再评价所带来的不可预计的数据和反馈。表中红色标注的部分是因为心血管安全性而导致撤市。
特非那丁,它是一种长效抗组胺药物,1982年首先在英、法、西德上市,1985年美国获准上市,以后得到迅速推广,在世界范围内广泛使用,用于治疗过敏性鼻炎。该药是第一个用于缓解过敏症状而不引起嗜睡的抗组胺药。在1990年报告第一例治疗剂量引起的死亡病例,同时大量的患者出现心律失常副作用后,FDA不得不给特非那定加上了心律失常副作用的警告;在1992年共收集到15例死亡病例和83例尖端扭转室速(TdP)病例,FDA再次升级为严重的“黑框警告”;在1997年已经引起大约350例死亡,FDA最终将特非那丁撤出市场,结束了这个原创药的生命。
为什么会这样?这是由于当时药物学家对hERG抑制几乎没什么认识,根本没考虑到要对特非那定进行心脏毒性的测试,也就不可能发现特非那定分子本身对钾离子通道有较强的抑制作用(即hERG抑制)。
之后,为了避免上述严重不良事件的发生,欧美药物监管部门要求制药企业在新药研发阶段全面评估药物潜在的心脏毒性。
同时,ICH于2000 年11 月发布“S7A: Safety Pharmacology Studies for Human Pharmaceuticals”指南,其明确提出药物的安全性评价要包括对心脏复极和QT 间期的影响;
在2005年发布“S7B:The Nonclinical Evaluation of the Potential for Delayed Ventricular Repolarization(QT Interval Prolongation) By Human Pharmaceuticals”指南,这是对S7A 的补充,提出了临床前评价的方法包括4 个水平上的模型,当中的第一条就是:在动物或人类的离体心肌细胞或转染HERG表达的通道上,进行评价药物对快速激活延迟整流钾电流(IKr)的影响;
在2006年提出“E14: The Clinical Evaluation of QT/QTc Interval Prolongation and Proarrhythmic Potential for Non-Antiarrhythmic Drugs”指南,要求对所有作用于全身的新药进行全面QT 研究,定量评估候选药物对QT 间期的影响。
2014年我国发布《药物QT间期延长潜在作用非临床研究技术指导原则》也对药物非临床研究作出了规定。迄今,我国尚未发布QT间期临床研究技术指导原则。
在临床上,药物导致的QT 延长引起的尖端扭转性室性心动过速也是引起了越来越多的重视。2010 年AHA/ ACC 公布了院内预防尖端扭转性室性心动过速的指南,当中明确提出了QT 间期延长诱发的尖端扭转性室性心动过速是严重的恶性心律失常,必须采取积极措施进行防治。可见,在临床前及临床上评价药物对心肌复极的影响已经达成了共识,国内外的药物管理机构和临床医生对药物致QT 间期延长的副作用有着极大的重视。
以上所颁布的关于心脏QT间期延长的指南根本目的是为了在新药研发的早期阶段评价化合物是否具有心脏风险,从而降低后期研发风险。自2005 年发布ICH E14/S7B 指导原则以来,没有已上市药物再因QT相关不良反应而导致撤市,同时上市后非抗心律失常药物导致TdP的报告也显著减少。但是,该指南依然存在局限性。一方面,hERG通道阻滞不是QT间期延长的唯一因素,另一方面,QT 间期延长并不一定导致TdP。
第二部分:心脏安全性的评价方法
2.1 正常心电图与QT间期
由窦房结发出的冲动,通过心肌传导系统产生心肌自律细胞和收缩细胞除极化和复极化的连续过程,引起一系列的电位改变,用体表电极记录下来,就成为心电图。
所谓心脏的QT间期,是指从QRS波群开始到T波结束的一段时间,包括心室去极化和复极化的过程,QT间期延长正受到越来越多的关注,并且被认为是新药安全性评价的关键指标之一。QT间期延长,容易导致恶性心律失常风险增加,最常引发尖端扭转型室性心动过速(TdP),而TdP易演变成心室纤颤并导致猝死。
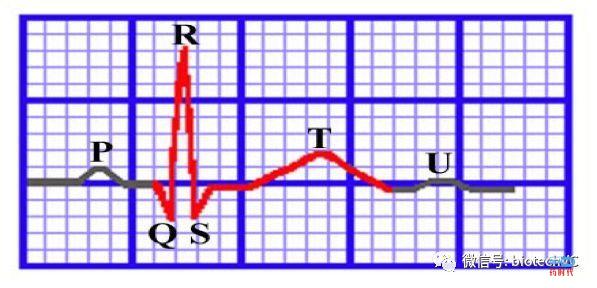
正常心电图(红色段为QT间期)
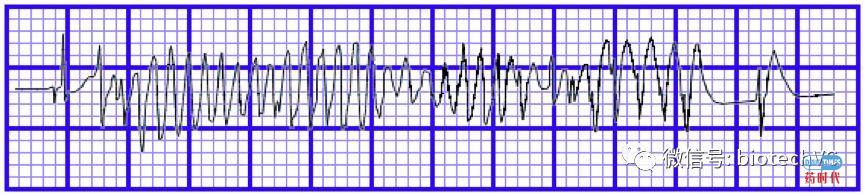
TdP(尖端扭转型室性心动过速)
2.2 心肌细胞膜电生理变化
心电图的形成是基于心肌细胞的除极和复极过程中电位的变化。而在静息状态时,膜内电位负于膜外,约为-90mV,即处于极化状态。当心肌细胞受到刺激而兴奋时,膜电位发生改变,形成动作电位。
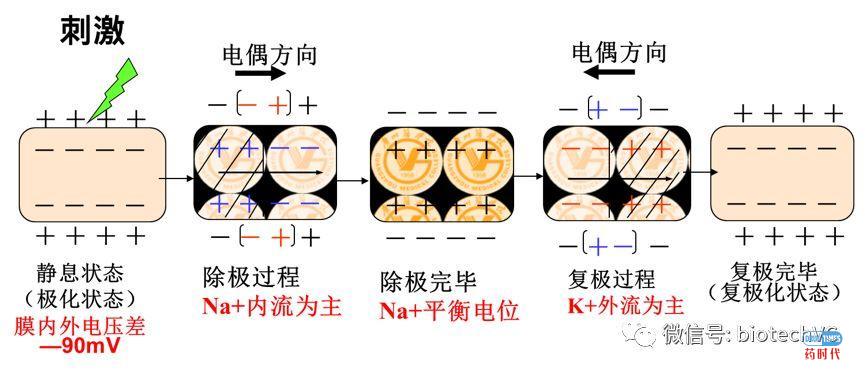
(心肌细胞除极与复极过程)
2.3 hERG基因与编码蛋白通道
hERG基因最初是由Warmke等在1994年从人类海马cDNA文库中分离鉴定得出的[2],与果蝇EAG基因具有同源性。hERG基因位于人7号染色体上(7q35~q36),约55kb,有16个外显子,编码1159个氨基酸残基。它可在人身体组织心肌、脑、肝脏、脾脏等中均有表达,其中在心肌组织中表达最高。hERG基因编码的蛋白产物是心肌组织中关键的膜结合钾离子通道的内孔形成部分,受膜电位控制并以门控方式调节钾离子流出细胞。当化合物结合到hERG钾通道内,导致钾离子外流受阻,可延长心肌细胞复极化时间,反映在心电图中即QT间期延长,进而可能诱发TdP的致命风险。

(hERG基因编码的K离子通道蛋白产物)
hERG抑制分为遗传性(原发性)和非遗传性(继发性)两类。遗传性QT间期延长主要包括能产生离子通道功能障碍的基因突变及先天性QT间期延长综合征;非遗传性QT间期延长可由代谢异常、疾病及药物所致引起的。
1995年,Sanguinetti等首次通过在细胞上转染hERG基因表达hERG蛋白的通道,也证实了单纯hERG 基因表达的hERG 通道,其生物学特性与正常的IKr通道完全一致[3]。这也就是现在采用转染hERG 基因的细胞体外评价药物对IKr的影响的理论基础。
2.4 如何评价药物对hERG通道电流的影响?
理论上,对hERG通道电流最理想的方法是在心肌细胞上直接测定IKr,但这存在着很多问题:
(1)应用酶解法急性分离心肌细胞要求要较高的技术和花费的时间较多,在消化的同时,也可能部分消化了钾通道蛋白[4];
(2)心肌细胞除了IKr外,还有很多钠、钙电流等,这些电流会混淆IKr;
(3)心肌具有收缩性,对钙的反应灵敏,因此在膜片钳记录时要形成非常好的高阻封接才能进行电流测定[5]。
相反,如何能利用hERG基因在合适的细胞上表达hERG电流,进而测定药物对快速延长整流钾电流的影响,似乎成了一种更好的选择。因此,根据ICH S7B指南要求评价药物是否阻断IKr,可以在分离的心肌细胞上进行直接测定IKr或者在转染hERG基因的细胞上测定hERG电流。
最早,分别采用爪蟾卵母细胞和中国地鼠卵巢细胞(CHO)转染hERG基因表达钾通道电流,发现前者比后者表达的钾电流要高[6-7];同时,这两种细胞都为异源性细胞,和人细胞还存在着种族的差异。因此,1996年Snyders等首次提出采用HEK293细胞可以稳定地表达hERG基因[8],如今已成为可靠的体外评价方法被广泛应用。
2.5 hERG 抑制体外评价技术及影响因素
膜片钳技术被称为研究离子通道的“金标准”,是研究离子通道的最重要的技术。随着研究的不断深入,目前膜片钳技术已从常规膜片钳技术发展到全自动膜片钳技术和FluxORTM Thallium Assay等,用来研究化合物与离子通道作用的作用机制,也用于新药申报过程中候选药物的毒性评价和先导化合物的结构优化。
在评价药物对电流强度的抑制效应时,最主要的一个指标是半数抑制浓度IC50,该指标一般要求对多个浓度的药物进行测定(5-8个细胞/浓度),然后用Hill方程拟合得到。
因此,该指标的测定过程中不可避免地存在着很多影响因素,包括但不限于以下方面:(1)实验的温度可影响IC50;(2)不同的电压刺激方案也会影响IC50的结果;(3)实验的细胞载体也会影响IC59;(4)用于测定的电极内液、细胞外液的影响。所以,这就提醒我们在评价药物对hERG电流的影响时,首先要保证实验条件的一致性,才能获得更加客观、正确的药物抑制效应。
比如,之前我们考察的几个项目,其hERG IC50两次测定结果相差3倍以上,是因为这是来自于两个不同的实验室所测。
第三部分:hERG IC50与心脏安全性的关联性分析
通过以上方法获得hERG IC 50值,如何去评价其与心脏安全性的关系呢?我们来看三篇文献进行分析。
第一篇文章是Redfern WS于2003年发表的《Relationships between preclinical cardiac electrophysiology, clinical QT interval prolongation and torsade de pointes for a broad range of drugs: evidence for a provisional safety margin in drug development》。这篇文章共纳入100个药物,并按照TdP发生频率分为五大类。经过分析后,最终结果显示hERG IC50超过治疗的最高游离血药浓度30倍是相对安全的范围,不会发生致心律失常作用。
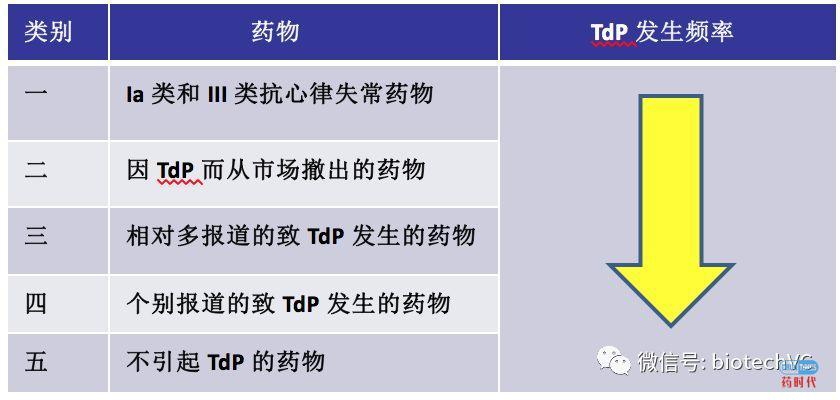
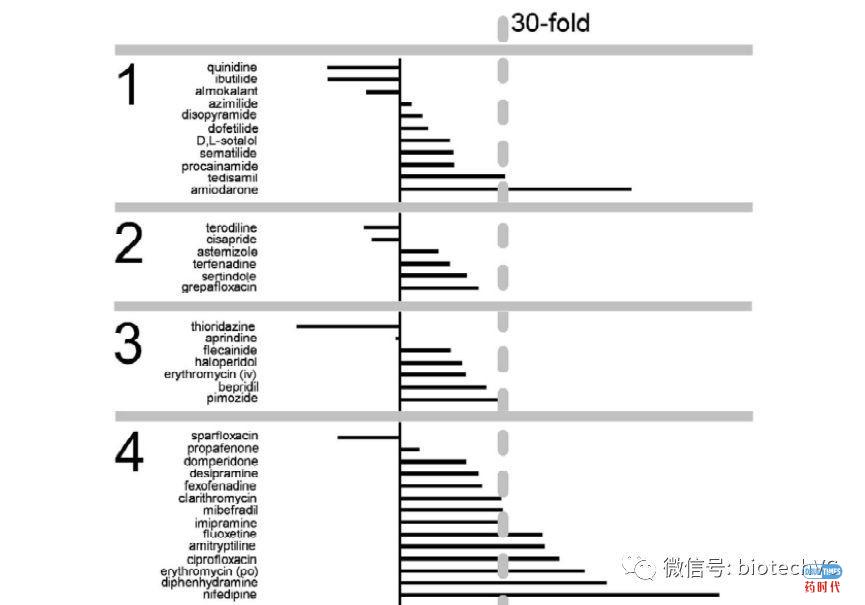
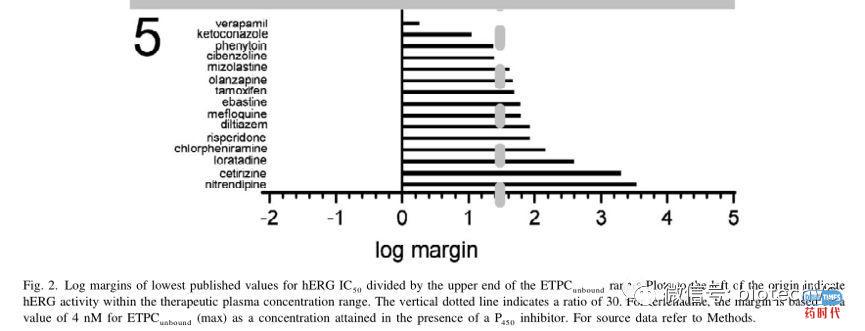
此外,该文章并提出安全界限也要反映不同疾病的严重程度和医学需求:
对于如果不给予治疗就会死亡的疾病,如肿瘤,AIDS,一些感染性疾病等,HERG IC50是Cmax的10倍可认为是安全的;
对于较为严重的疾病,如中风、帕金森病、精神分裂症、癫痫症、哮喘症、关节炎等,30倍可以认为是安全的;
对于较轻的疾病,如雷诺病、季节性鼻炎、湿疹等,100倍甚至更高的倍数才可认为是安全的;对于抗精神病药物,因患者可能会超量服用,也应该是100倍是合适的。此外,还必须考虑治疗目标、患者人数和给药途径的变化。
第二篇文章是Charlotte van Noord在2011年发表的《Non-cardiovascular drugs that inhibit hERG-encoded potassium channels and risk of sudden cardiac death》。该文章共纳入了1424例猝死患者和14443例对照组病例,回归分析结果显示:HERG IC50/ 游离血药浓度(ETCPunbound)≤30时,药物致TdP的发生率高;相反,HERG IC50/ ETCPunbound>30时,药物致TdP的发生相对少。此研究同样证实了30倍的标准可以作为衡量药物致TdP发生的相对危险。
第三篇文章是Christopher E. Pollard 于2017年发表的《An Analysis of the Relationship Between Preclinical and Clinical QT Interval-Related Data》。该文章共研究了24个小分子药物的临床QT间期数据(13个QT间期延长,11个QT间期正常),并研究了对狗QT间期影响和hERG IC50值,最终通过三个维度分别计算敏感性与特异性来评价结果的一致性。
维度一:hERG IC50绝对值
hERG IC50 <10uM时,13个临床QT间期延长的药物中检测出7个;
hERG IC50 >10uM时,11个无临床QT间期延长的药物中检测出10个。
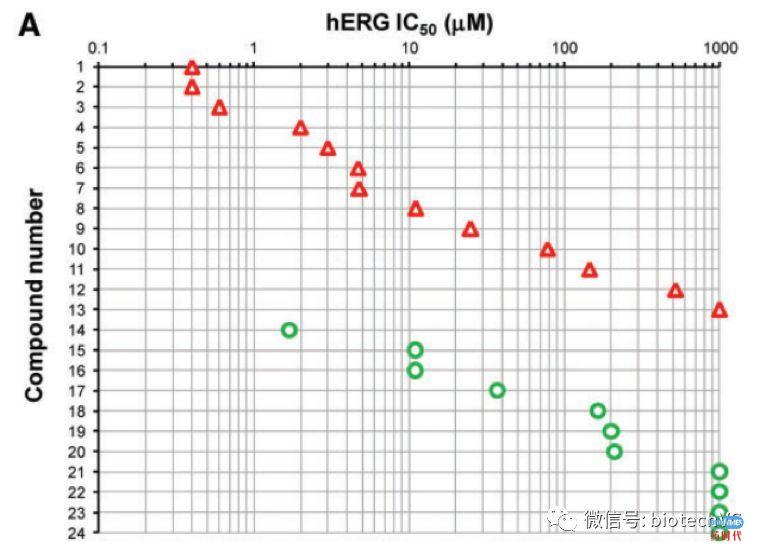
(红色代表QTc延长,绿色代表无QTc延长)
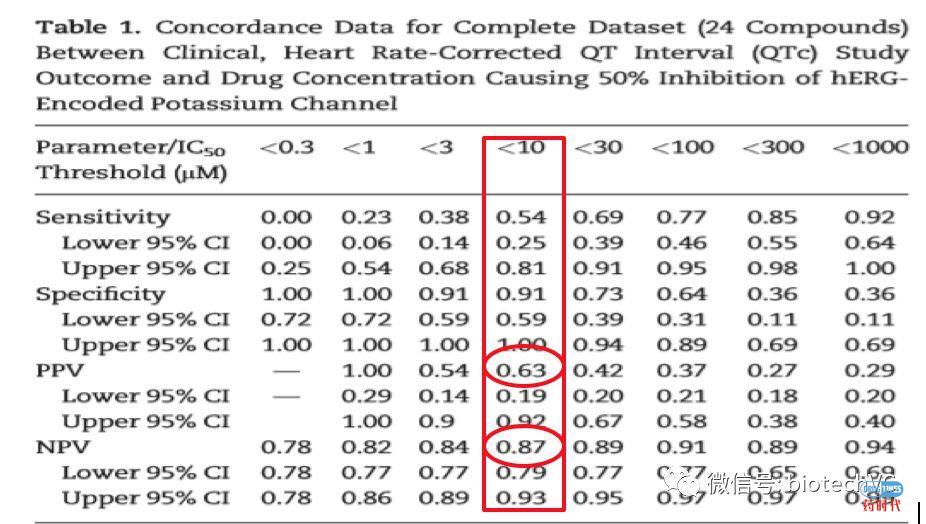
以上数据得出:敏感性和特异性之间的最佳平衡发生在hERG IC50=10uM,此时PPV和NPV分别是0.63与0.87。
维度二:安全界限 Safety Margin=hERG IC50/ 游离Cmax
safety margins <30-fold,13个临床QT间期延长的药物中检测出9个;
safety margins >30-fold,11个无临床QT间期延长的药物中检测出10个。
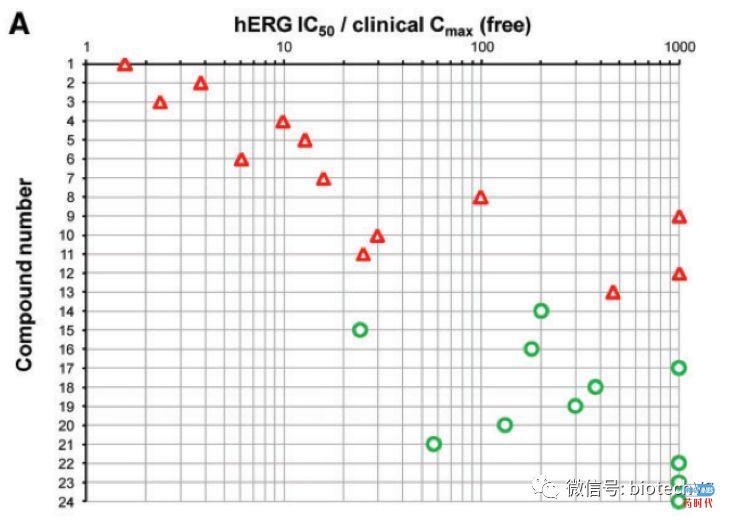
(红色代表QTc延长,绿色代表无QTc延长)
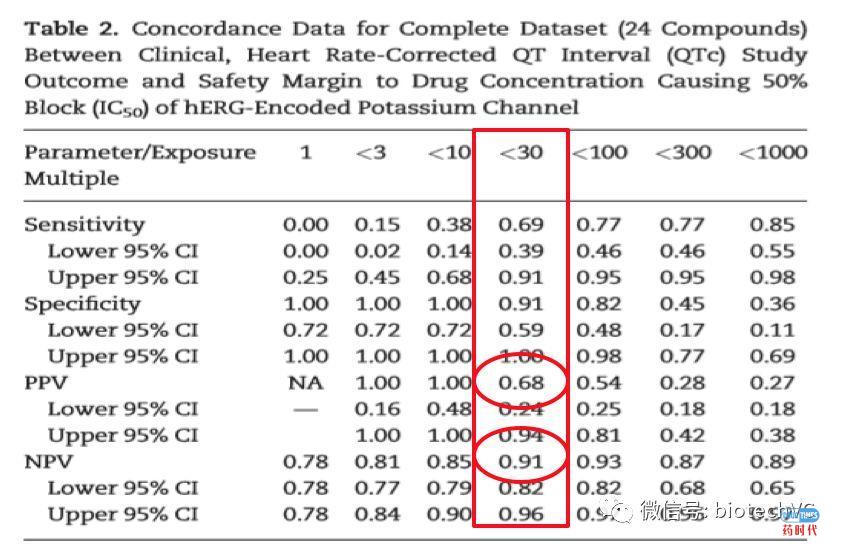
以上数据得出:敏感性和特异性之间的最佳平衡发生在hERG IC50/ free clinical Cmax =30-fold,此时PPV和NPV分别是0.68与0.91。
维度三:dog Cmax(free)/clinical Cmax(free)
dog Cmax(free)/clinical Cmax(free)= 10-fold,13个临床QT间期延长的药物中能延长狗QT间期共检测出8个;
dog Cmax(free)/clinical Cmax(free)= 10-fold,11个无临床QT间期延长的药物中未延长狗QT间期共检测出10个。
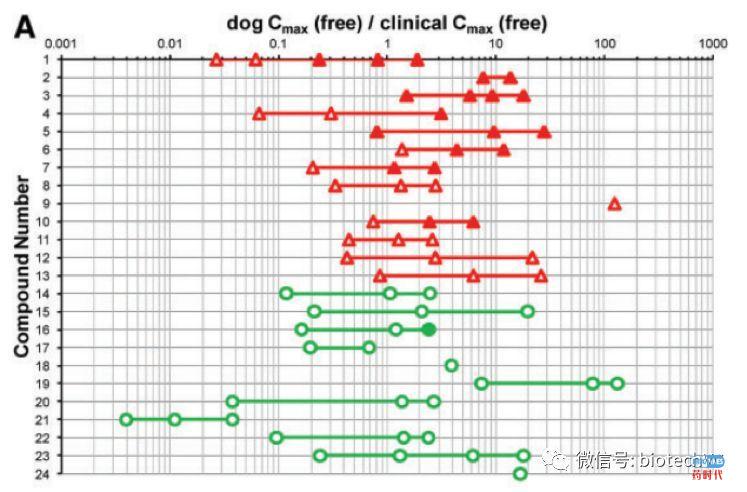
Filled symbols indicate that there was a QTc increase in dogs
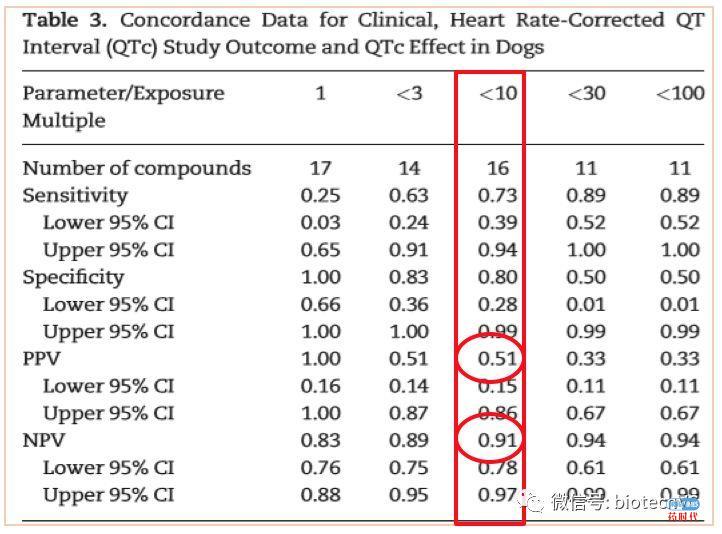
以上数据得出:敏感性和特异性之间的最佳平衡发生在dog Cmax free/clinical Cmax free =10-fold,此时PPV和NPV分别是0.51与0.91。
综合以上信息,在评估hERG IC50与心脏安全性之间的关系时,可以分为绝对值(hERG IC50)和相对值(hERG IC50/Cmax(free)两个指标评估分析。但正如其他评价化合物成药性的数据一样,hERG IC50并不是终止化合物开发的唯一准则,应多方综合考虑。
如果对本文感兴趣,可以加微信youxuanzibenlifang,欢迎提出批评、建议和不同意见交流。
以下视频为心肌细胞膜电位变化视频
最后,如果你觉得本文尚可一读,还请转发朋友圈,让更多的朋友能获得新的启发。
扫描下方二维码,关注我们BiotechVC的订阅号。

以上文字由Biotech venture capital原创,仅为促进讨论与交流,不构成法律意见或咨询建议。版权所有,违者必究。如需转载,请注明作者和Biotech venture capital原创。
过往文章:
参考文献:
[1]Zamorano JL, Lancellotti P, Rodriguez Muñoz D, et al. 2016 ESC Position Paper on cancer treatments and cardiovascular toxicity developed under the auspices of the ESC Committee for Practice Guidelines:The Task Force for cancer treatments and cardiovascular toxicity of the European Society of Cardiology (ESC) [J].Eur Heart J, 2016, 37(36): 2768-2801. DOI: 10.1093/eurheartj/ehw211.
[2]. Warmke JW, Ganetzky B. A family of potassium channel genes related to eag in Drosophila and mammals. Proc Natl Acad Sci U S A 1994;91(8):3438-42.
[3]. Sanguinetti MC, Jiang C, Curran ME, Keating MT. A mechanistic link between an inherited and an acquired cardiac arrhythmia: HERG encodes the IKr potassium channel. Cell 1995;81(2):299-307.
[4]. 黄兴福,杨艳敏,戴研等. 盐酸关附甲素对转染HERG 基因表达的快速激活延迟整流钾通道电流的影响. 中华心律失常学杂志2008;12(3):169-74.
[5]. Hancox JC, McPate MJ, El Harchi A, Zhang YH. The hERG potassium channel and hERG screening for drug-induced torsades de pointes. Pharmacol Ther 2008;119(2):118-32. 6
[6]. Witchel HJ, Milnes JT, Mitcheson JS, Hancox JC. Troubleshooting problems with in vitro screening of drugs for QT interval prolongation using HERG K+ channels expressed in mammalian cell lines and Xenopus oocytes. J Pharmacol Toxicol Methods 2002;48(2):65-80.
[7]. Engeland B, Neu A, Ludwig J, Roeper J, Pongs O. Cloning and functional expression of rat ether-a-go-go-like K+ channel genes. J Physiol 1998;513 ( Pt 3):647-54.
[8]. Snyders DJ, Chaudhary A. High affinity open channel block by dofetilide of HERG expressed in a human cell line. Mol Pharmacol 1996;49(6):949-55.
视频剪辑来源:Crash Course. ( 2015, March 2 ). The Nervous System, Part 2 – Action! Potential!: Crash Course A&P #9 [Video file].
发布者:药时代,转载请首先联系contact@drugtimes.cn获得授权

 为好文打赏 支持药时代 共创新未来!
为好文打赏 支持药时代 共创新未来! 
