Hello,各位小伙伴,我们今天继续,不做铺垫,直接上货。
单抗Asn297处的糖基化模式调节了抗体Fc结构域与Fc受体结合的构象状态。 这些N-聚糖对FcγR结合位点的结构完整性至关重要,已经证明糖基化的去除消除了FcγR亲和力和补体结合/效应功能。目前已经证实减少岩藻糖和唾液酸基团并增加二等分N-乙酰葡糖胺,半乳糖和甘露糖可增强Fc介导的ADCC和CDC效应。
下面我们来看几个临床上成功的例子。
mogamulizumab是一种靶向CC趋化因子受体4型(CCR4)的人源化单克隆抗体,被FDA批准用于复发或难治性CCR4阳性T细胞白血病或淋巴瘤的患者的治疗。obinutuzumab(GA101,Gazyva),是一种含有N-乙酰葡糖胺的非岩藻糖基化抗CD20单抗药物,Obinutuzumab于2013年被批准用于治疗先前未治疗的慢性淋巴细胞白血病(CLL)患者。
与第一代产品利妥昔单抗(美罗华)相比,第二代产品obinutuzumab去除了50%的盐藻糖修饰并包含二等分N-乙酰葡糖胺,对人FcγRIII的亲和力较第一代产品高50倍,其对表达CD20的淋巴瘤细胞系的ADCC效应增加了10-100倍,在临床上也体现了治疗的优越性。
目前国内天广实开发了第3代产品MIL62,MIL62是利妥昔单抗(美罗华)与阿托珠单抗(GA101)的优效产品(me-better)。MIL62是100%岩藻糖敲除的第三代CD20抗体,目前体外药效学证明有效于进口产品美罗华。
第三个例子是benralizumab(Fasenra),该抗体是人源化的非岩藻糖基化的抗IL-5Rα抗体,其介导与表达IL-5Rα的嗜酸性粒细胞的ADCC消耗效应显著,所述嗜酸性粒细胞涉及哮喘急性发作。Reed等人通过临床研究发现通过单次静脉注射benralizumab(MEDI-563)就可以导致轻度哮喘患者嗜酸性粒细胞的强烈消耗,效果可以持续8-12周。
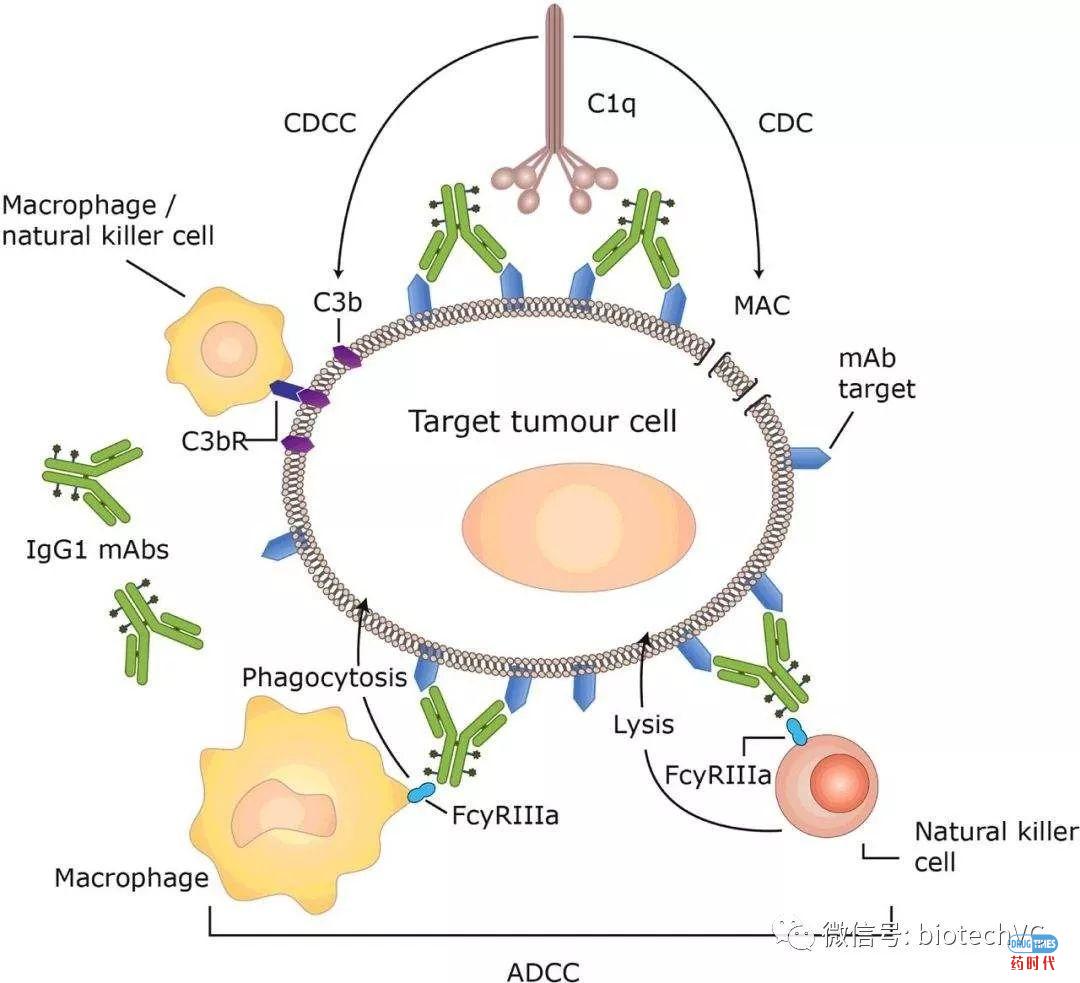
抗体Fc区域的氨基酸突变改造
通过于抗体Fc结构域中引入氨基酸的点突变可以增强抗体Fc效应功能。该方法不仅仅限于对FcγRIII的改变,还允许突变Fc结构域中与多个活化FcγR有关的区域。
一系列已上市治疗性单抗药物(利妥昔单抗,西妥昔单抗,曲妥珠单抗和阿仑单抗)的Fc区域的突变体显示出FcγRIIIA亲和力的增加及FcγRIIB亲和力的降低,这些抗体Fc区域的双突变体(Ser239Asp / Ile332Glu)和三联突变体(Ser239Asp / Ile332Glu / Ala330Leu)增强了ADCC活性。 这些突变体在临床前体外实验中显示出2个数量级的体外效应功能增强,能够作用于表达低水平靶抗原的细胞,并在体内临床前模型中显示出细胞毒性效力的增强,当然这些突变体的临床疗效还需要进一步证实。
几项临床前研究同样也表明Fc蛋白工程化单克隆抗体对癌症和病毒的体内活性增强,目前这些单克隆抗体已进入临床开发阶段,例如治疗白血病的CD19抗体 Xmab5574(MOR00208),用于治疗乳腺癌的HER2抗体margetuximab。
此外我们还可以突变抗体Fc片段的Gly236Ala以增强抗体药物的ADCP活性,其选择性地增强对FcγRIIA的亲和力,通过Gly236Ala突变(巨噬细胞介导的ADCP和NK细胞介导的ADCC)以及Ser239Asp / Ile332Glu双突变的联合(ADCC增强)进一步增强抗体的效应功能。
此外,位于上铰链区的突变可以增强与C1q的结合以增强抗体的CDC活性。其他位置的点突变,如CH2结构域中的Lys326Trp和Glu333Ala,已被证明可以增强CDC效应。 双突变体,如Lys326Trp / Glu333Ala,Lys326Ala / Glu333Ala和Lys326Met / Glu333Ser,以及三重突变体,如Ser267Glu / His268Phe / Ser324Thr,与单个突变相比,其抗体的CDC效应进一步增加。
设计新功能抗体
新功能抗体药物是当前及未来抗体药物开发的一个重要方向,通过开发新功能抗体来提高抗体药物的疗效,新功能抗体主要有抗体偶联药物(ADC),双特异性抗体,纳米抗体,Fab片段,ScFv结构的抗体,抗体融合蛋白等。这些抗体的特点和优势大家从很多公开资料中都能了解,这里就不再详细阐述。简而言之,开发这些抗体的最终目的还是希望提高抗体药物的效应功能,使抗体药物的临床疗效提升或副作用改善从而实现较已有药物差异化的竞争优势。
为了实现上述目标,我们应从哪些方面去努力呢?总的来看有两个重要的方面:
(1)首先应该进行详细和充分的文献、专利调研,仔细分析研究目标抗体及对应靶标涉及到的全部文献及专利材料,例如目前针对这一抗体及作用靶点已经开展了哪些研究,哪些方面是未研究的,为什么没有相关的研究,在针对该靶点的抗体药物设计方面哪些是可以近一步改进和提高的,以及这些改进和提高对于提高临床疗效及减少副作用的关系有多大,对于以上方面的理解深度将会影响抗体药物的后续开发,要出色的完成上述工作对于相关人员的知识储备和经验的积累也具有很高的要求;
(2)要求抗体药物研发人员对抗体整体及各部分的结构功能有很深的理解,此外还需要对不同类型的IgG抗体的结构有清晰的认识,清楚的明白关键结构域中每一个氨基酸的变化对于抗体结构和功能的影响,并能综合运用现有的各种方法手段进行分析验证。在上述基础上用多种不同的体内外模型对相关设计进行多次重复验证,此外抗体各部分连接的氨基酸也很重要,连接linker的稳定性,连接序列的刚性及柔性的组合策略,不同氨基酸的搭配组合,充分考虑所用氨基酸的电荷性质等等。做到上述这些方面,往往会使我们设计的抗体在疗效上体现出一个意想不到的提升效果。
以上我们用较大的篇幅分析了抗体药物研发的第一方面的重要变化:抗体药物的副作用及功能和疗效的提升方面。
下边我们看看文章开篇提到的第二个方面:单抗药物作用靶标不断扩大已拓展到新的疾病治疗领域和新的适应症。
抗体药物的靶标可以分为已经成药的靶标和未成药的靶标,对于已经成药的靶点来说,由于有大量的科学和临床研究,而且有已经上市的药物,对于作用于这类靶点的抗体,临床开发研究的风险较小,我们可以认为靶标的生物学风险基本已经去除,但对于开发针对此类靶点的抗体药物来说,后期商业化的风险较大。对于抗体研发企业来说能否开发出具有比较优势的差异化产品至关重要,这个差异化主要体现临床疗效的提升和副作用的降低方面,这也就回到了我们第一部分探讨的内容上。
对于未成药的靶标而言还可以细分为两大类。
(1)一类靶标相对比较成熟,目前有大量的基础及临床相关的研究,有较多的人类循证医学的证据,目前已经有该靶点的抗体进入临床研究,这样的靶标虽然较有上市药物的成熟靶点的临床开发风险大,但是一旦开发成功,应该具有较大的商业价值。
(2)另一类靶标就是目前虽然有一些基础研究,但是临床和人类循证医学研究很少,目前也没有进入临床阶段的抗体,对于这样的靶标,临床开发风险极高,对于这样的靶点很多的时候还是保持一种跟踪的态度,在概念验证上作一些初步工作,对相关靶点的研究密切关注,如有重大突破就可以快速跟进。大家可能会问对于抗体药物的全新靶点(还未报到的靶点)我们是怎么发现的呢,我们可以通过分子流行病学调查,人类遗传学研究,人类功能基因组学、蛋白组学研究,生物信息学、药理学、模式动物研究,人类循证医学研究去发现。
总之,抗体药物的开发必须以临床需求为核心,解决还未满足的临床需求,不断开发新的靶点和适应症。对于初创型的抗体药物研发企业,需要有清晰的自我定位和目标,在抗体作用的靶标上选择好,可以兼顾不同类型靶点的一个搭配组合,确立好了相关的靶点后就需要在提升抗体药物功能和疗效上下功夫,特别是针对本文分析的抗体药物免疫源性及抗体药物副作用及效应功能,通过这些努力以提高抗体药物的临床疗效,要实现这些还需要抗体研发人员对于抗体药物的结构和功能的关系有深入的了解,需要抗体研发企业有较深的积累沉淀。
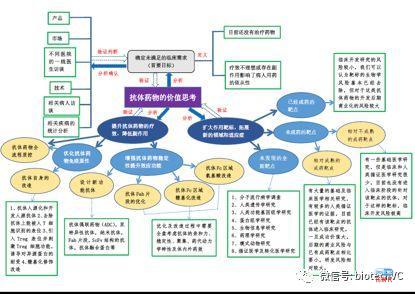
为了大家清理理解本文的思路和阐述的逻辑,特配思维导图一张供大家参考(如果需要清晰图片,关注公众号后,在消息栏输入“思维导图”即可)。
以上文字由Biotech venture capital原创,仅为促进讨论与交流,不构成法律意见或咨询建议。版权所有,违者必究。如需转载,请注明作者和Biotech venture capital原创。
参考文献:
Leipold D, Prabhu S. Pharmacokinetic and pharmacodynamic considerations in the design of therapeutic antibodies.Clin Transl Sci. 2018 Nov 10.
Chan AC Carter PJ. Therapeutic antibodies for autoimmunity and inflammation.Nat Rev Immunol,2010,10( 5) : 301-316.
Weiner L M,Surana R,Wang S.Monoclonal antibodies:Versatile platforms for cancer immunotherapy.Nat Rev Immunol,2010,10( 5) : 317-327.
Kozlowski S, Swann P Current and future issues in the manufacturing and development of monoclonal antibodies.Adv Drug Deliv Rev,2006,58( 5-6) : 707-722.
图片部分来自网络,部分为作者亲自画的,尤其是后面那个思维导图,我们独家IP,特公开分享给大家。
发布者:药时代,转载请首先联系contact@drugtimes.cn获得授权

 为好文打赏 支持药时代 共创新未来!
为好文打赏 支持药时代 共创新未来! 
