
在56位可评估疗效的MCL患者中,29位患者产生了应答,其中14位患者完全缓解(CR),15位患者部分缓解(PR),总体缓解率(ORR)为52% (95% CI: 38-65)。在先前接受过共价BTK抑制剂治疗的52患者中,ORR也达到了52% (95% CI: 38-66)。
在19位可评估的华氏巨球蛋白血症患者中,13位患者产生了应答,其中9位患者PR,4位患者为轻微缓解(MR),ORR为68% (95% CI: 44-87)。先前接受过共价BTK抑制剂的13位患者中,ORR为69% (95% CI: 39-91, 5位患者为PR, 4位患者为MR)。
在8位可评估疗效的滤泡性淋巴瘤患者中,有4位患者产生应答。
在8位Richter综合征患者中,有6位患者产生应答,ORR为75%。
在剩余的39位可评估疗效的患者中,有8位患者产生应答,其中6位为DLBCL(弥漫大B细胞细胞瘤)患者(6/25),2位为MZL(边缘区淋巴瘤)患者(2/9)。
LOXO-305在CLL和SLL中的表现
-
在121位疗效可评估的、接受过BTK抑制剂治疗的患者中,ORR为62% (95% CI: 53-71);而在接受10个月或以上随访的患者群体中,ORR达到84% (21/25)。,这种随着时间推移而加深的反应与其他BTK抑制剂是一致的,这表明LOXO-305的总体疗效将通过进一步的随访继续增强。
-
因疾病进展而停止使用共价BTK抑制剂的患者的ORR(67% [53/79])与因毒性或其他原因停药的患者的ORR (52% [22/42])相似。
-
BTK C481突变患者的ORR (71% [17/24])与未出现该突变患者的ORR相似(66% [43/65])。
-
在曾接受过化学免疫治疗、共价BTK抑制剂以及BCL-2抑制剂的患者中,ORR为69% (27/39)。
-
在曾接受过所有5类可用的CLL/SLL疗法(包括化学免疫疗法、共价BTK抑制剂、BCL-2抑制剂、PI3K抑制剂)患者中,ORR为58% (7/12)。
-
在28位17p缺失或TP53突变或两种情况都存在的患者中,ORR为79% (22/28)。
LOXO-305在BRUIN试验的安全性
LOXO-305的下一步计划
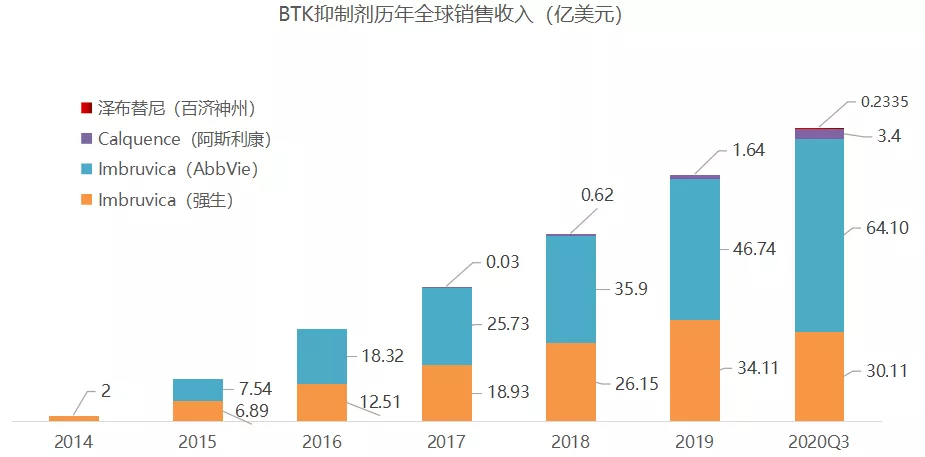
图片来源:参考资料3
参考资料
2、https://investor.lilly.com/news-releases/news-release-details/loxo-oncology-lilly-announces-updated-data-phase-12-bruin
3、https://mp.weixin.qq.com/s/86Af-lK0gFHuY0GbxUZHPQ
– END –
内容仅供感兴趣的个人谨慎参考,非商用,非医用、非投资用。 版权归拥有者。欢迎朋友们指正!衷心感谢! 荷包满满的赛诺菲能否靠另辟蹊径在BTK抑制剂竞赛中杀出重围? ASH | 三年过去了,历史上第一个获批的CAR-T疗法Kymriah如今有何进展?
 点击直达,每月2万多朋友到过这里!
点击直达,每月2万多朋友到过这里!
发布者:药时代,转载请首先联系contact@drugtimes.cn获得授权



 为好文打赏 支持药时代 共创新未来!
为好文打赏 支持药时代 共创新未来! 
