
⬆️欢迎参加2020中国NASH大会!
本文转自生命科学前沿,作者病毒学。点击阅读原文
2020年8月6日,Cell推出重磅级解析“SnapShot: Enveloped Virus Entry”,详细阐述病毒是如何进入细胞进行复制,进而感染人类引起疾病的。来自英国伯明翰大学、加拿大多伦多大学、美国加州拉荷亚免疫学研究所和加拿大安大略儿童医院的科研人员以包膜(或囊膜)病毒为例,深度剖析病毒入侵过程。
众所周知,为了成功启动感染程序,病毒必须将其基因组从一种宿主细胞或生物体传播或传递到另一种宿主细胞或生物体内。为此,包膜病毒必须首先将其膜与靶宿主的细胞膜融合。在此过程中,研究人员依照代表性病毒发生入侵行为的细节顺序重点介绍它们为进入宿主细胞胞质而使用的策略(尽管它们有许多不同之处,并且融合的位置各不相同,但包膜病毒进入和膜融合步骤的共同原理在很大程度是一致且保守的)。
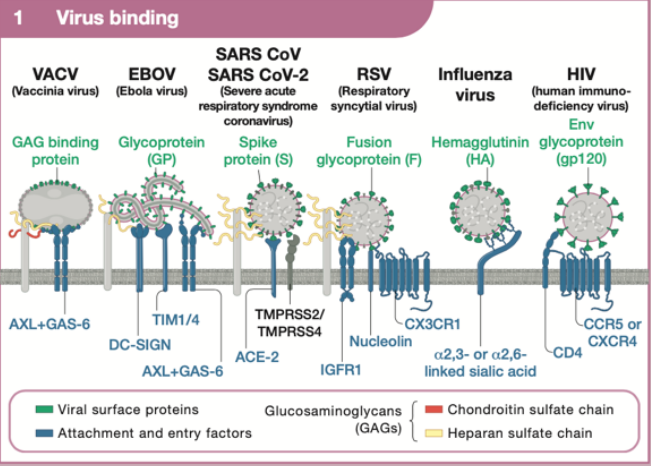
病毒吸附/粘附/结合
病毒受体可分为两大类:粘附/附着因子(attachment factors)和入侵/进入受体(entry receptors)。粘附因子会将病毒聚集在细胞表面,而入侵受体则是启动内吞作用(endocytosis)的真正信号蛋白。
硫酸软骨素和乙酰肝素蛋白聚糖(分别为CSPG和HSPG)是带负电荷的多糖,可作为大多数包膜病毒的典型附着因子。通过低亲和力、高活性的相互作用,这些聚糖促进了病毒结合以及随后与入侵受体的结合。入侵受体必须满足几个条件:它们必须与病毒接触,激活触发内吞作用的信号级联,并且对于病毒内化(internalization)至关重要(essential)。(补充:内吞(endocytosis)是指细胞外物质通过膜内陷和内化进入细胞的过程。内吞被认为是细胞对微粒作用的主要机制,所有真核细胞都具有内吞功能。)大多数病毒使用多重入侵受体,这些受体可以起到促进病毒蛋白质结构改变的作用,从而使共受体结合,将感染扩展到不同的细胞类型或宿主,或者同时下调宿主的免疫反应。
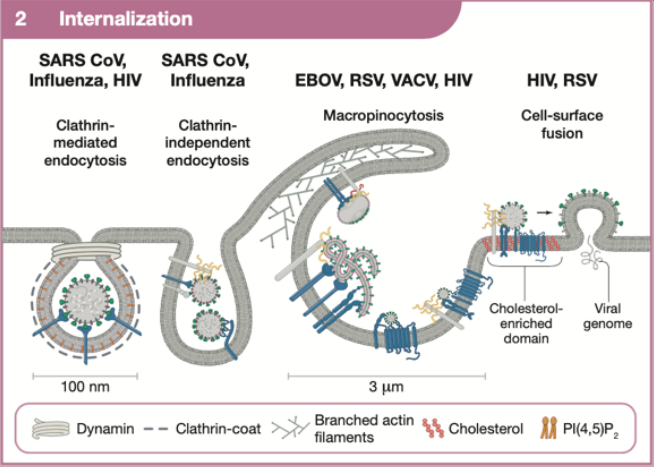
内化
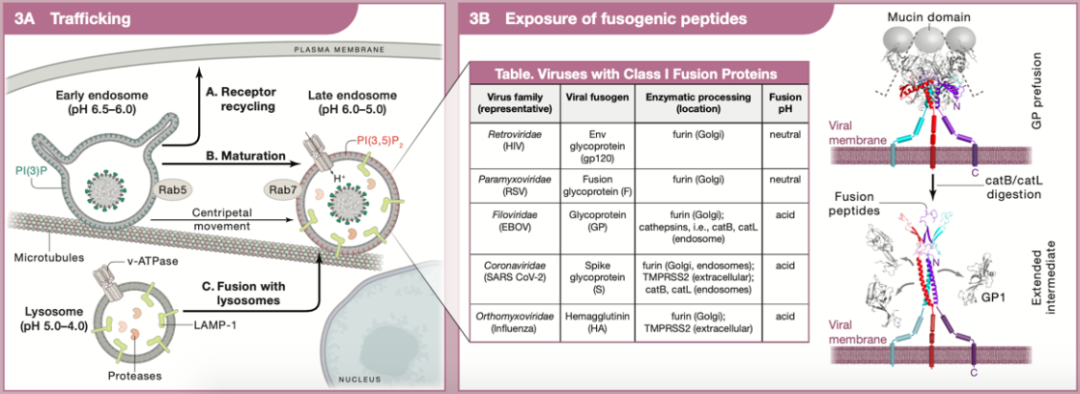
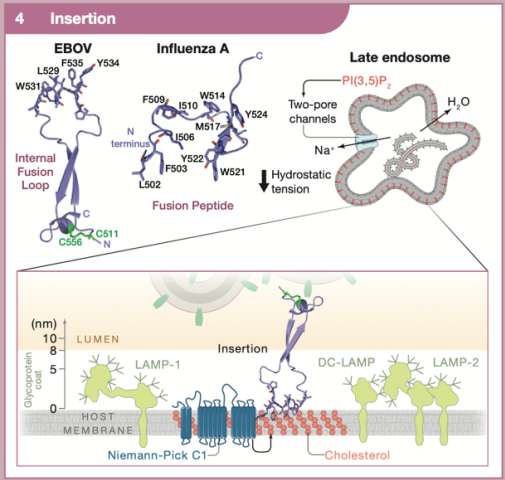
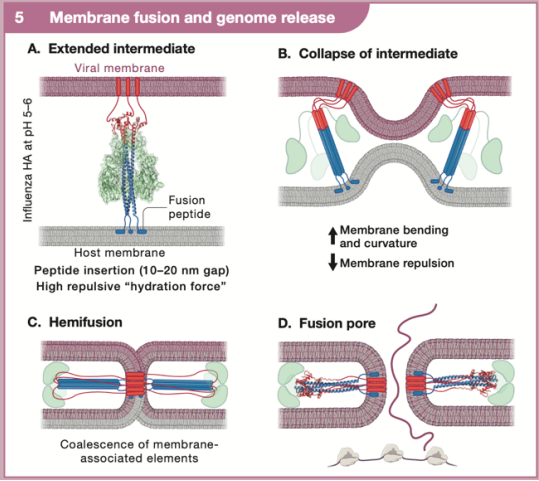
肽的插入导致双层之间的接触,称为延伸的中间产物(extended intermediate),但病毒膜和宿主膜之间仍然存在间隙,并且存在融合的高能屏障。为降低此屏障,插入的肽增加了宿主膜的排列秩序,病毒融合蛋白的大规模结构重排导致延伸的中间体塌陷,从而降低了对置膜的水合排斥力。融合还需要从溶酶体中挤出渗透物以减轻静水压力,该压力部分由脂质门控阳离子通道介导。病毒融合素的普遍特征是它们的两个膜相关元件(融合肽或环和跨膜锚)聚集在一起以促进融合孔的形成,病毒基因组通过融合孔释放到细胞质中。
参考文献:
DOI: http://dx.doi.org/10.1016/j.cell.2020.06.033。
-END-
免责声明
内容仅供感兴趣的个人谨慎参考,非商用,非医用、非投资用。版权归作者。衷心感谢!
本文为转载,药时代持中立态度,请理性阅读
版权声明:文中图片取自网络,根据CC0协议使用,版权归拥有者。
任何问题,请与我们联系。衷心感谢!
重启7年的诺华神经科学部门7.95亿美元下注Sangamo锌指蛋白转录因子
峰回路转——从临床暂停到P<0.001,CymaBay对PBC和NASH领域仍抱有信心


本文转载自生命科学前沿,本文观点不代表药时代DrugTimes立场。



 为好文打赏 支持药时代 共创新未来!
为好文打赏 支持药时代 共创新未来! 
