
⬆️ 欢迎参加2020中国NASH大会!
本文转自药渡,作者药渡咨询郭雷团队,点击阅读原文
干细胞分类
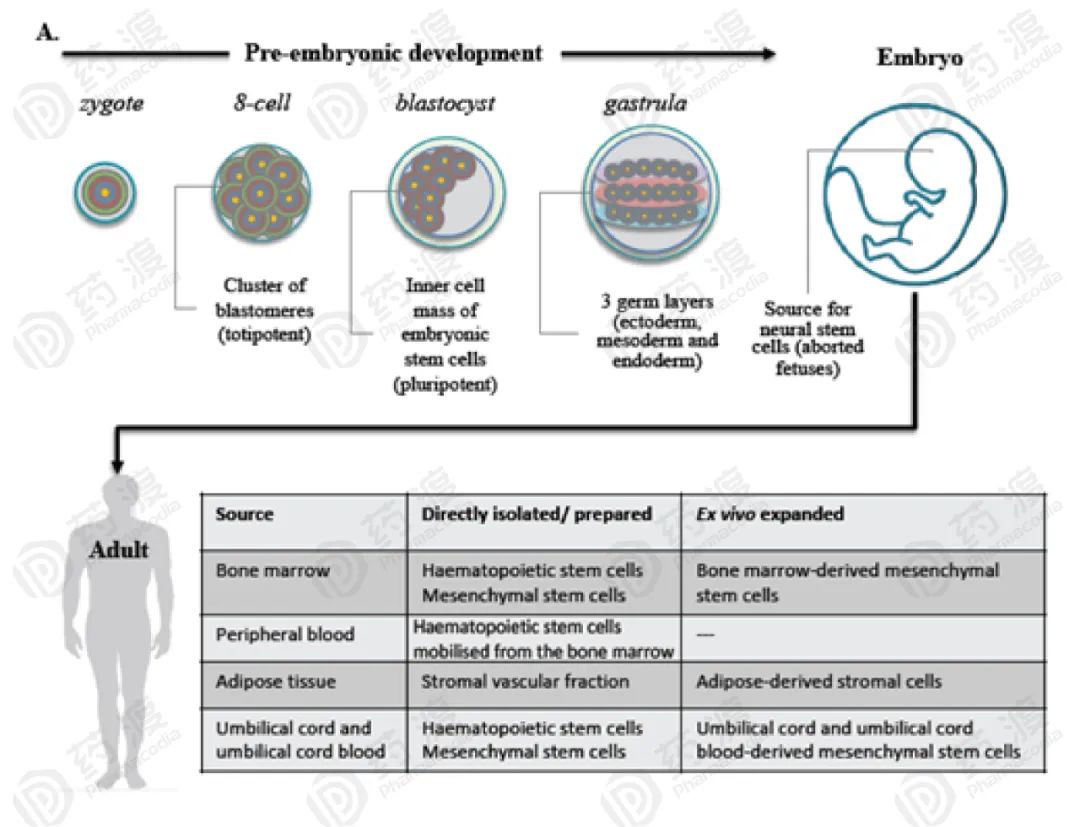
临床进展
干细胞治疗在中枢神经性疾病上的进展
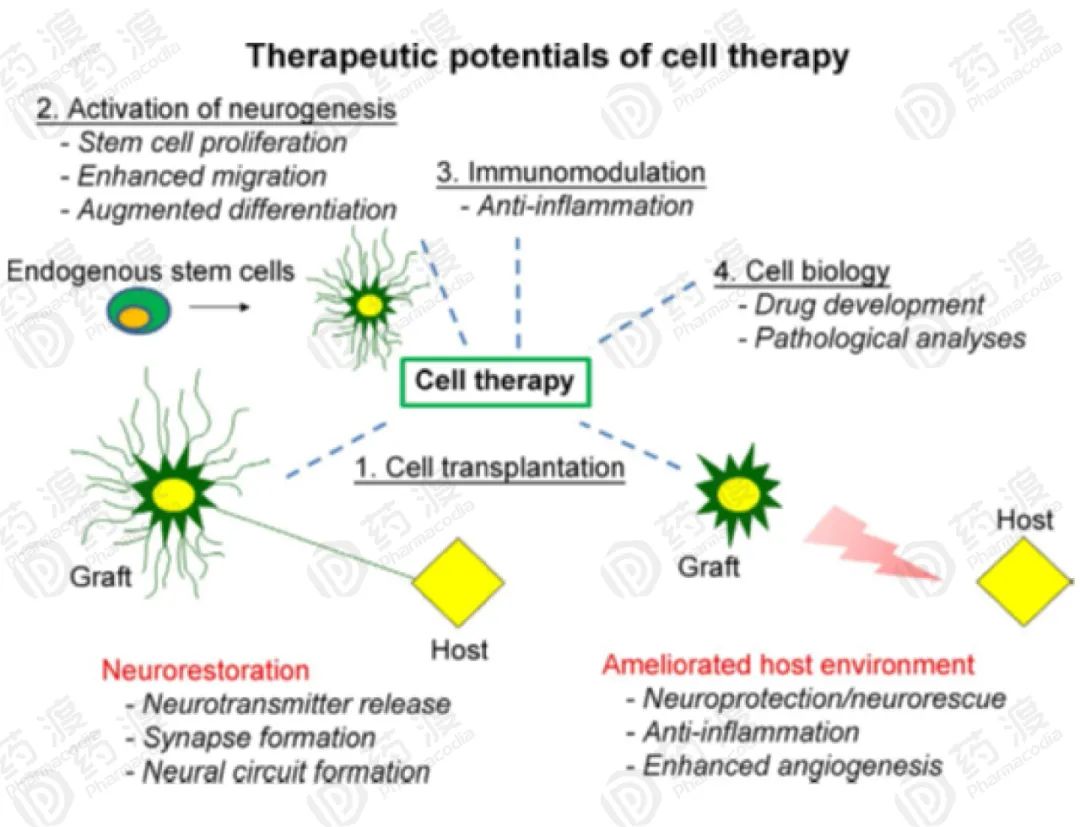
干细胞治疗神经性疾病上的困难
总结
参考文献
2. Brown C, McKee C, Bakshi S, et al. Mesenchymal stem cells: Cell therapy and regeneration potential. J Tissue Eng Regen Med. 2019;13(9):1738-1755. doi:10.1002/term.2914
3. Yasuhara T, Kawauchi S, Kin K, et al. Cell therapy for central nervous system disorders: Current obstacles to progress. CNS Neurosci Ther. 2020;26(6):595-602. doi:10.1111/cns.13247
4. Aly RM. Current state of stem cell-based therapies: an overview. Stem Cell Investig. 2020;7:8.Published 2020 May 15. doi:10.21037/sci-2020-001
– END –
免责声明
内容仅供感兴趣的个人谨慎参考,非商用,非医用、非投资用。版权归作者。衷心感谢!
本文为转载,药时代持中立态度,请理性阅读
版权声明:文中图片取自网络,根据CC0协议使用,版权归拥有者。
任何问题,请与我们联系。衷心感谢!
Fiona Yu专栏 | 兼并界鼻祖葛兰素,300多岁能否再次回春?

本文转载自药渡,本文观点不代表药时代DrugTimes立场。


 为好文打赏 支持药时代 共创新未来!
为好文打赏 支持药时代 共创新未来! 
