
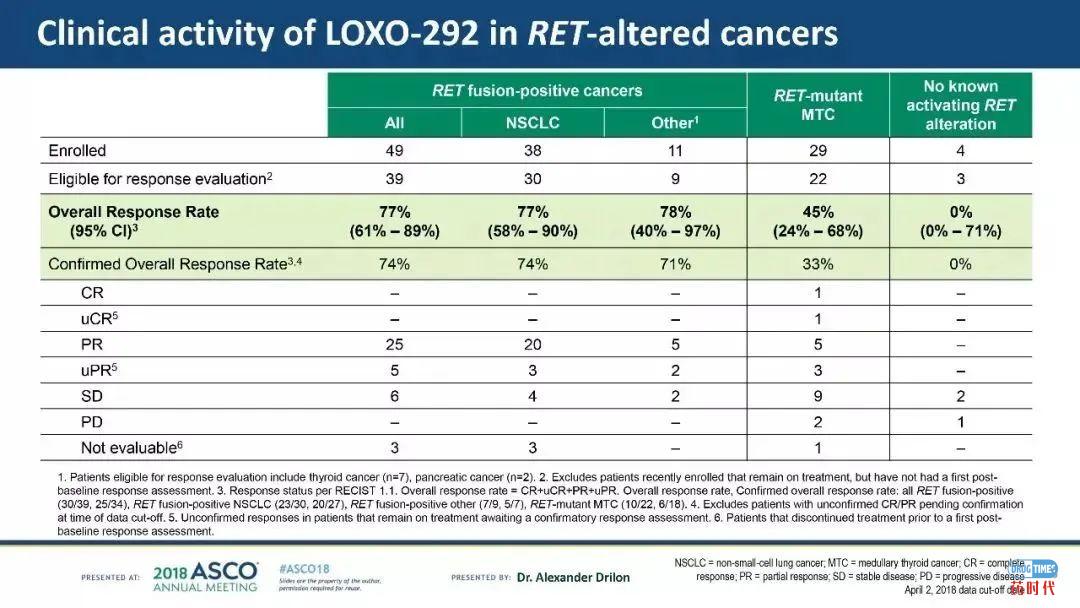
这款疗效卓群的药物并没有辜负大众的殷殷期望,它凭借LIBRETTO-001试验中积极的临床数据在2020年1月又获得FDA的优先审评资格。就在所有人猜测这款药物是否会在2020年第三季度上市时,中国时间2020年5月9日(美国时间2020年5月8日),FDA发布公告,批准了Retevmo™适用于转移性RET融合阳性非小细胞肺癌、晚期或转移性RET突变甲状腺髓样癌和晚期或转移性RET融合阳性甲状腺癌。
1、杰出的治疗疗效
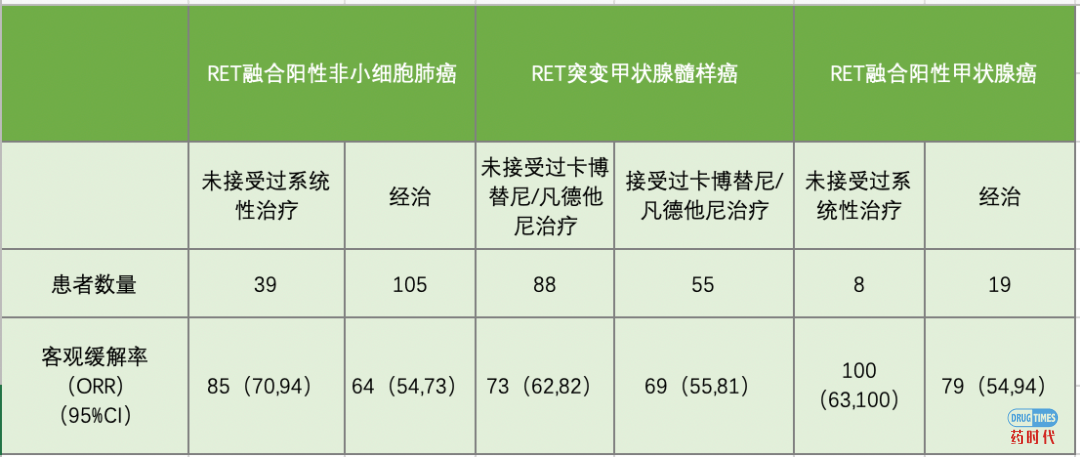
3、关于甲状腺癌的治疗:疗效方面,RET融合的甲状腺癌,未接受过系统性治疗的ORR 100%,经治的ORR 79%。
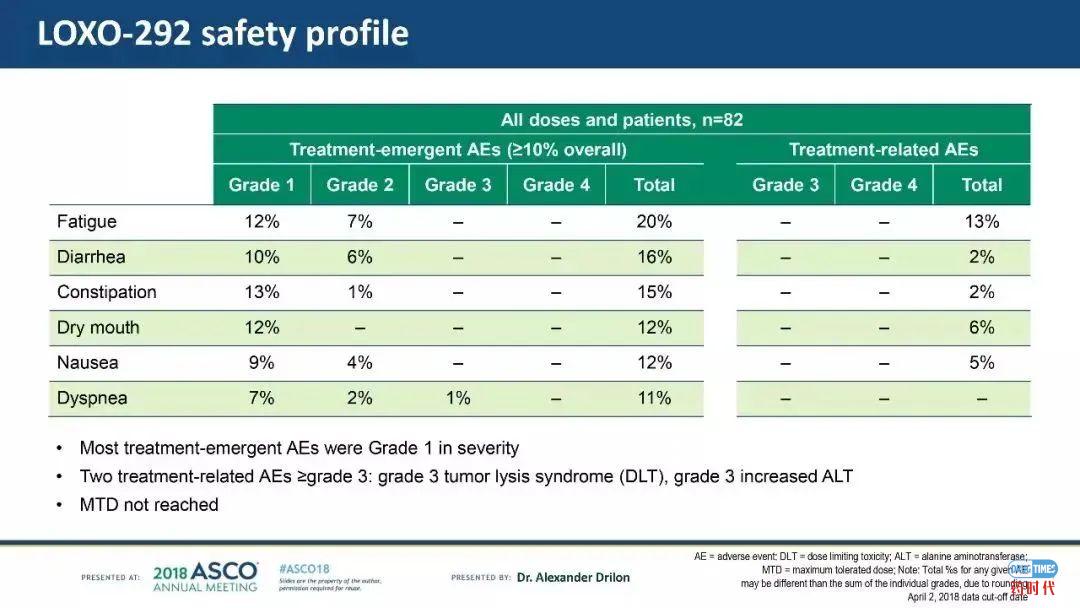
2、良好的安全性数据
 图1、源自药物临床试验登记与信息公示平台[5]
图1、源自药物临床试验登记与信息公示平台[5]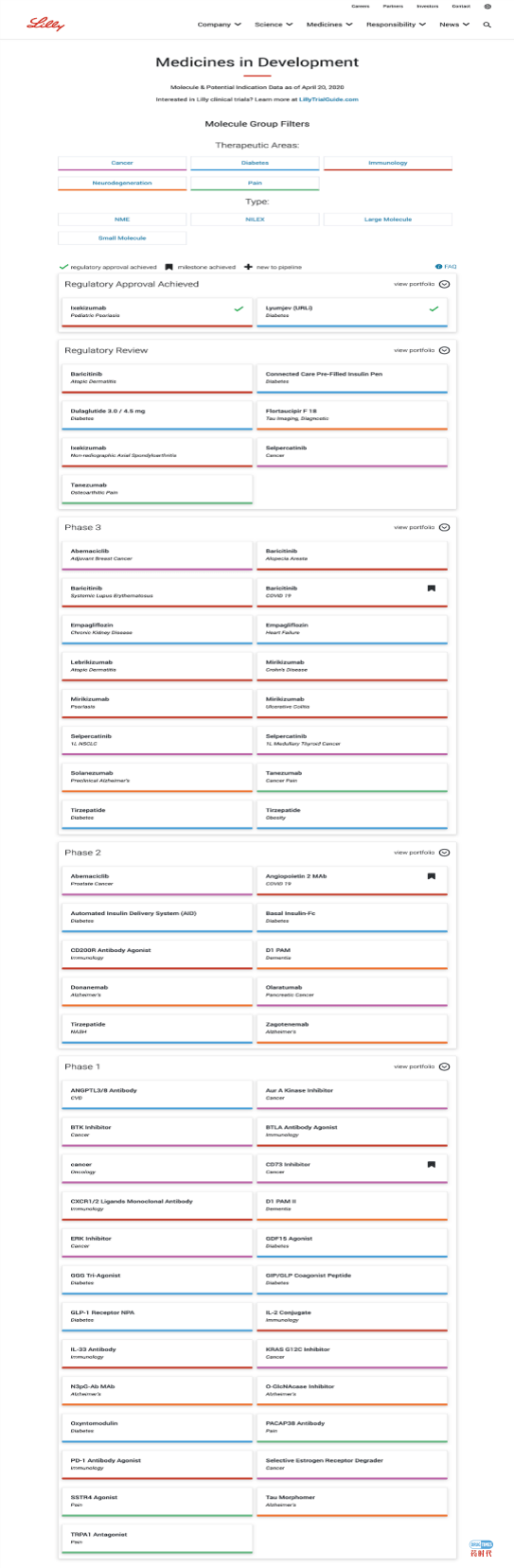
1、内部研发
2、内外合作
3、外部兼并
参考文献
2、抗癌路漫漫其修远兮RET是一个重要的抗癌分子靶点
3、2018ASCO第二天 | 新型RET靶向药Loxo-292震撼来袭!
4、LOXO-292靶向RET变异,Loxo新药获FDA突破性疗法认定
5、药物临床试验登记与信息公示平台
6、礼来与和黄中国医药在中国开展肿瘤药物研发及运营合作
7、和记黄埔与礼来携手将爱优特推向市场,价格已流出
8、达伯舒®(信迪利单抗注射液)联合力比泰®(注射用培美曲塞二钠)和铂类治疗一线非鳞状非小细胞肺癌(nsqNSCLC)3期ORIENT-11研究达到主要研究终点
达伯舒®(信迪利单抗注射液)联合健择®(注射用吉西他滨)和铂类化疗一线治疗鳞状非小细胞肺癌III期研究达到主要研究终点
达伯舒®(信迪利单抗注射液)二线治疗晚期食管鳞癌的临床研究达到主要研究终点
9、重磅 | 礼来制药与君实生物就新冠肺炎合作开发预防与治疗性抗体疗法
10、礼来11亿美元收购Dermira 获两款皮肤病治疗药物
版权声明:文中图片取自网络,根据CC0协议使用,版权归拥有者。
任何问题,请与我们联系。衷心感谢!
并购小故事 | 礼来和Loxo如何用18天达成价值80亿美元的“闪婚”?
礼来宣布Basaglar®(甘精胰岛素)治疗中国成年1型糖尿病患者的III期临床研究达到主要研究终点

发布者:药时代,转载请首先联系contact@drugtimes.cn获得授权

 为好文打赏 支持药时代 共创新未来!
为好文打赏 支持药时代 共创新未来! 
